2-метилбутен
Cтраница 1
Исходный 2-метилбутен - 3-ол - 2 получают гидрированием продукта присоединения ацетилена к ацетону ( см. гл. [1]
Димеризация 2-метилбутена - 2 в присутствии серной кислоты приводит к различным олефинам. [2]
Выход 2-метилбутена - 1 снижается при повышении температуры обработки цеолитов NaY и NaM в токе воздуха и проходит через минимум при повышении температуры обработки водородом. Сравнение зависимостей выхода 2-метилбутена - 1 ( см. рис. 1.19) иизопентана ( см. рис. 1.18) от условий термообработки цеолитов указывает на антибвтный характер связи между величинами выходов этих продуктов реакции в исследованных условиях. Это можно объяснить тем, что с повышением гидрирующей активности катализатора 2-метилбутен - 1, образующийся в результате изомеризации 2-метилбутена - 2, также подвергается гидрированию, вследствие чего уменьшается его содержание в продуктах реакции. [3]
Гидроборирование 2-метилбутена - 1 приводит к спирту, энантиомерная чистота которого в 4 раза выше, чем в случае аналогичной реакции 2-фенилпропена. Так как замещение а-пинена в случае обоих олефинов происходит приблизительно в одинаковой степени, то. [4]
Гидрирование 2-метилбутена - 2, присутствовавшего в исходной смеси, протекало в незначительной степени, поэтому оценить кинетический изотопный эффект достаточно точно для этой реакции не представлялось возможным. Выше при обсуждении результатов исследования гидрирования 2-метилбутена - 2 было показано, что изомеризация двойной связи в этом углеводороде протекает как независимо от реакции гидрирования, по-видимому, на бренстедовских кислотных центрах, образующихся в результате частичного декатионирования Na-формы цеолита в процессе его приготовления, так и одновременно с реакцией гидрирования, вероятно, на гидрирующих активных центрах катализатора через общее промежуточное полугидрированное состояние. Поскольку в обоих случаях изомеризация осуществляется путем последовательного присоединения и отщепления ионов водорода ( Н при изомеризации на кислотных центрах и Н - при гидрировании), то это и является причиной близких величин наблюдаемых изотопных эффектов реакций гидрирования и изомеризации. [5]
Смесь 2-метилбутена - 2 и З - метилбутапола-2; в) М - нит-розоди-егор-бутиламин; г) я-нитрозо - Л - метил - Л - зтор-бутилани-лин; д) п-нитрозо - Л Д - диэтиланилин; е) Л - нитрозо - А - метилани-лин; ж) л1 - нитробензолдиазонийхлорид; з) / г-метилбензолдиазо-нийхлорид; и) ЛМштрозодифенилашш, легко перегруппировывающийся в п-нитрозодифениламнн. [6]
Выход 2-метилбутена - 1 снижается при повышении температуры обработки цеолитов NaY и NaM в токе воздуха и проходит через минимум при повышении температуры обработки водородом. Сравнение зависимостей выхода 2-метилбутена - 1 ( см. рис. 1.19) низопентана ( см. рис. 1.18) от условий термообработки цеолитов указывает на антибатный характер связи между величинами выходов этих продуктов реакции в исследованных условиях. Это можно объяснить тем, что с повышением гидрирующей активности катализатора 2-метилбутен - 1, образующийся в результате изомеризации 2-метилбутена - 2, также подвергается гидрированию, вследствие чего уменьшается его содержание в продуктах реакции. [7]
Гидрирование 2-метилбутена - 2, присутствовавшего в исходной смеси, протекало в незначительной степени, поэтому оценить кинетический изотопный эффект достаточно точно для этой реакции не представлялось возможным. Выше при обсуждении результатов исследования гидрирования 2-метилбутена - 2 было показано, что изомеризация двойной связи в этом углеводороде протекает как независимо от реакции гидрирования, по-видимому, на бренстедовских кислотных центрах, образующихся в результате частичного декатионирования Na-формы цеолита в процессе его приготовления, так и одновременно с реакцией гидрирования, вероятно, на гидрирующих активных центрах катализатора через общее промежуточное полугидрированное состояние. Поскольку в обоих случаях изомеризация осуществляется путем последовательного присоединения и отщепления ионов водорода ( Н при изомеризации на кислотных центрах и Н - при гидрировании), то это и является причиной близких величин наблюдаемых изотопных эффектов реакций гидрирования и изомеризации. [8]
К 2-метилбутену - 2 присоединяют бромистый водород против правила Марковникова. Полученный З - бром-2 - метилбутан нагревают со спиртовым раствором мочевины. Образовавшуюся соль S-алкилизотиурония гидролизуют щелочью в меркаптан ( см. Общий практикум по органической химии, стр. [9]
В 2-метилбутене - 2 отсутствует С - С-связь, необходимая для алкильного распада; в этом случае рвется связь С - Н и образуются ионы с массой 69, количество которых зависит от температуры эмиттера, что указывает на участие поверхности в реакции отрыва водорода. [10]
Изопентены - 2-метилбутен - 1, 2-метилбутен - 2, З - метилбутен-1 - являются важнейшим сырьем для получения изопрена. Многочисленные исследования [53] показали, что метод дегидрогенизации изо-пентенов до изопрена ( 725) является наиболее дешевым и перспективным. Одно из преимуществ этого метода - наличие большого запаса дешевого сырья, в отличие от других методов, которые в качестве сырья применяют ацетон и ацетилен или изобутилен и формальдегид. Метод дегидрогенизации основан на применении в качестве сырья изопентана, выделенного из газового бензина и изопен-танов, полученных в процессах термокаталитической переработки средних и тяжелых парафиновых углеводородов ( термический или каталитический крекинг), или в процессе каталитической дегидрогенизации фракции Cfi, выделенной из газового бензина. [11]
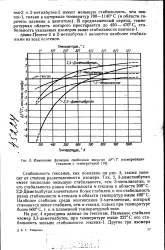 |
Изменение функции свободной энергии AF / 7 изомеризации гексанов с температурой. [12] |
Пентен-2 и 2-метилбутен - 1 являются наиболее стабильными из всех пентенов. [13]
Подействуйте на 2-метилбутен - 1 бромистым водородом и затем металлическим натрием. [14]
Триметилэтилен ( 2-метилбутен - 2) может быть дегидрирован в пентадиены при кратковременном ( 0 03 - 0 5 сек. Изопрен отделяют от побочных продуктов ( метана и бутилена) перегонкой. [15]
Страницы: 1 2 3 4