Результат - поляризационное измерение
Cтраница 1
 |
Схематические катодная ( 1 и анодная ( 2 поляризационные кривые, характеризующие активное растворение металла в кислоте. р - коррозионный потенциал, i K - скорость коррозии. [1] |
Результаты поляризационных измерений при анодном растворении металлов могут зависеть также от наличия в растворе нейтральных молекул, в частности органических веществ. [2]
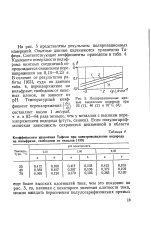
Результаты поляризационных измерений приведены в таблице. [3]
 |
Зависимость между числом оборотов электрода и. [4] |
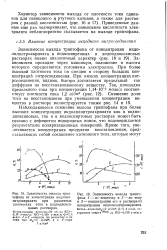
Результаты поляризационных измерений подтверждают проводившуюся ранее аналогию между действием перемешивания электролита в прикатодном слое на процесс формирования пленки и растворяющим действием сульфат-ионов. Однако эта аналогия отсутствует в условиях, когда пленка на катоде сформировалась и протекают обе реакции восстановления Сг6 - Сг3 и Cr6 - - Gr. [5]
Прогнозы из анализа результатов поляризационных измерений подтверждаются данными, полученными при непосредственном изучении влияния плотности тока, концентрации деполяризатора, и концентрации серной кислоты на скорость образования метаниловой кислоты. Детальное обсуждение результатов предполагается после получения кинетических данных для других электродных материалов. [6]
 |
Поляризационные кривые выделения водорода при 25 ( 1, 40 ( 2 и 70 С ( 3. [7] |
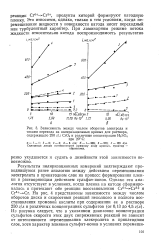
На рис. 5 представлены результаты поляризационных измерений. Опытные данные подчиняются уравнению Та-феля. Удаление с поверхности вольфрама окисных соединений со - q 8 провождается снижением перенапряжения на 0 13 - 0 23 в. [8]
Изменение состояния пассивирующей пленки и активной поверхности электрода в зависимости от условий электролиза должно влиять не только на результаты поляризационных измерений, но также и на данные, полученные другими методами, как, например, определением емкости двойного электрического слоя. [9]
Указанные обстоятельства дают, на наш взгляд, основание считать, что выводы о механизме разряда ионов из цианистых электролитов, сделанные из результатов поляризационных измерений [8, 61], не выходят за предел предположений гипотетического характера. В качестве одного из основных критериев предполагаемого механизма электродного процесса обычно используется величина предлогарифмического коэффициента Ъ в уравнении Тафеля. Однако эта величина не всегда может служить достаточно обоснованным аргументом в пользу определенного механизма. [10]
Наблюдающееся снижение выхода триптофана при более высоких концентрациях индолилнитроакрилата как в воднодиоксановых, так и в водноспиртовых растворах может быть связано с дефицитом водородных ионов, что подтверждается результатами поляризационных измерений. [12]
 |
Поляризационные кривые для реакции выделения водорода на различных металлах из кислых растворов. [13] |
На рис. 19.1 приведены поляризационные кривые для реакции выделения водорода из кислых растворов электролитов на электродах из разных металлов. Результаты поляризационных измерений очень чувствительны к условиям опыта, в частности, к степени чистоты поверхности электрода и раствора; по этой причине данные разных авторов заметно расходятся. [14]
В то же время возможность обнаружения и идентификации промежуточных низковалентных частиц индия, результаты количественного изучения закономерностей их образования при протекании электродных процессов и, в частности, повышение концентрации ионов одновалентного индия при анодной поляризации позволили убедительно доказать справедливость того предположения о равновесном характере стадии In: In e, которое лежит в основе указанного стадийного механизма. Таким образом, сопоставление результатов поляризационных измерений с непосредственным обнаружением промежуточных низковалентных частиц в ходе электродного процесса позволило всесторонне и однозначно обосновать стадийный механизм для индиевого электрода. Аналогичный подход позволил доказать стадийность процесса разряда-ионизации меди [ 177, 177а ] и может быть использован для выявления механизма других сложных электродных процессов. [15]
Страницы: 1 2