Результат - поляризационное измерение
Cтраница 2
Гетерогенные превращения пероксида водорода на углеродных материалах включают целый ряд реакций, протекающих как по химическому, так и по электрохимическому механизму. В качестве примера на рис. 60 сопоставлены результаты газометрических и поляризационных измерений в щелочном растворе пероксида водорода. Скорость этого процесса слабо зависит от потенциала. [16]
Более наглядным примером растворения электрода в щелочном растворе, закономерности которого могут быть объяснены при предположении о химическом механизме, является травление кремния в концентрированной щелочи. Как показали Изидинов, Борисова и Веселовский [233], в этом случае прежде всего наблюдается явное несоответствие между скоростью выделения водорода в отсутствие внешнего тока ( являющейся мерой скорости саморастворения кремния) и значением скорости саморастворения, найденной из результатов поляризационных измерений. Кроме того, в широкой области потенциалов при катодной поляризации скорость выделения водорода не зависит от потенциала, значительно превышает рассчитанную по соответствующим катодным токам и совпадает со скоростью выделения водорода в отсутствие внешнего тока. [17]
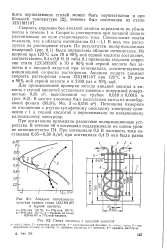 |
Схема змеевика с анодной защитой. [18] |
Специальные опыты показали, что в области потенциалов 0 1 - 1 1 В весь ток расходуется на растворение стали. По результатам поляризационных измерений ( рис. 8.1) были определены области потенциалов. Их ширина при 120 С для 70 и 90 % - ной серной кислоты составляет, соответственно, 0 4 и 0 8 В. В табл. 8.1 приведены скорости коррозии стали 12Х18Н10Т в 70 и 90 % - ной серной кислоте без защиты и с анодной защитой при потенциалах, соответствующих минимальной скорости растворения. Анодная защита снижает скорость растворения стали 12Х18Н10Т при 120 С в 24 раза в 90 % - ной серной кислоте и в 2300 раз в 70 % - ной. [19]
В подавляющем большинстве случаев наибольшее значение имеют блокировочный, или механический, коэффициент у3 и адсорбционный, или двойнослойный, коэффициент Y - Ь кинетические коэффициенты YI и Y2 обычно мало отличаются от единицы. Так как YS и Y4 можно найти не прибегая к прямым коррозионным измерениям, то появляется возможность теоретического расчета коэффициента торможения. Сопоставление расчетных коэффициентов торможения ( YTCOP) кислотной коррозии железа и цинка с полученными экспериментально ( Yancn) приведено в табл. 24.1. Необходимые для расчета значения коэффициентов переноса заимствовались из результатов поляризационных измерений, величины 6 ( степень покрытия поверхности металла ингибитором) брались средними из данных трех независимых методов, изменение Дг з принималось равным смещению максимума электрокапиллярной кривой в присутствии данной концентрации ингибитора - хлорида децил-3 - оксипи-ридиния. Расхождение между расчетными и опытными значениями коэффициентов не превосходит обычных ошибок коррозионных измерений. [20]
В подавляющем большинстве случаев наибольшее значение имеют блокировочный, или механический, коэффициент уз и адсорбционный, или двойнослойный, коэффициент у-ь кинетические коэффициенты YI и 2 обычно мало отличаются от единицы. Так как уз и 74 можно найти не прибегая к прямым коррозионным измерениям, то появляется возможность теоретического расчета коэффициента торможения. Сопоставление расчетных коэффициентов торможения ( утеор) кислотной коррозии железа и цинка с полученными экспериментально ( уэксп) приведено в табл. 24.1. Необходимые для расчета значения коэффициентов переноса заимствовались из результатов поляризационных измерений, величины 6 ( степень покрытия поверхности металла ингибитором) брались средними из данных трех независимых методов, изменение Дг) принималось равным смещению максимума электрокапиллярной кривой в присутствии данной концентрации ингибитора - хлорида децил-3 - оксипи-ридиния. Расхождение между расчетными и опытными значениями коэффициентов не превосходит обычных ошибок коррозионных измерений. [21]
Однако при этом следует помнить, что сопротивление электролита внутр. К тому же уменьшение диаметра зонда связано еще с трудностями изготовления и обращения с ним. Поэтому применение очень тонких зондов часто становится невозможным. На рис. 6 показаны результаты поляризационных измерений, проведенных зондами новой конструкции ( рис. 5) с разными величинами внешних диаметров. Это доказывает, что при тщательной калибровке конечные результаты измерения не зависят от диаметра зонда и что для измерения поляризации достаточно поляризующихся электродов вполне можно применять зонды диаметром в несколько миллиметров. [22]
У этих ионов нет никакой возможности рекомбинировать вновь, поскольку оба сорта ионов задерживаются в пространственно разделенных местах. Эти ионы являются избыточными по отношению к тем, которые имеются при тепловом равновесии. На величину тока они не оказывают пока большого влияния, поскольку уже близко подошли к соответствующим электродам и не вносят существенного вклада в его величину. Но если изменить его направление, то они сразу же получают возможность принимать участие в электрическом токе, двигаясь через весь кристалл на другую его сторону. В этот момент проводимость увеличивается, что со всей убедительностью вытекает из табл. 5, содержащей результаты поляризационных измерений и представляющей собой продолжение таблицы на стр. [23]
Вероятно, ни один из классов координационных соединений не был предметом таких многочисленных спектроскопических исследований, как комплексы металлов с окисью углерода и соответствующие соединения с изоэлектронным цианидным лиган-дом. Выполнены многочисленные расчеты нормальных колебаний этих молекул и ионов, отличающиеся высокой степенью строгости и полнотой. Очевидно, что использование спектров КР должно оказать существенную помощь в этих исследованиях. Тетраэдрические комплексы М ( СО) 4 имеют девять нормальных колебаний ( 2Ai - j - 2E - - F - - 4F2), из которых четыре ( F2) активны в ИК-спектре и восемь ( 2А - - 2Е 4F2) - в спектре КР. Для октаэдрических карбонилов М ( СО) е из общего числа колебаний ( 2Alg 2Eg Flg 4Flu 2F2g 2F2u) четыре ( Flu) активны в ИК-спектре и шесть ( A g, Eg и F2g) - в спектре КР-Кроме того, частоты всех фундаментальных колебаний, за исключением валентных колебаний С-О, располагаются обычно ниже 750 см-1, и это сильно усложняет отнесение частот. Таким образом, надежное отнесение колебаний этих комплексов невозможно без полных данных по ИК - и КР-спектрам, включая результаты поляризационных измерений. [24]
Страницы: 1 2