Vb-группа
Cтраница 1
У элементов VB-группы наблюдается общая для всех cf - элементов особенность изменения фундаментальных характеристик атомов, таких, как атомные и ионные радиусы, потенциалы ионизации и ОЭО. [1]
Простые вещества элементов VB-группы - тугоплавкие, кор-розионностойкие металлы, не реагируют с кислотами-неокислите-лями. Смесь HNOs и НС1 ( царская водка) превращает ванадий в УСЦ. Хлорид ванадия ( 1У) - красно-коричневая неполярная жидкость, водой частично гидролизуется с образованием хлорида ванадила ( УО) СЬ. Высший хлорид ванадия не существует. [2]
Большая устойчивость соединений с низшей степенью окисления у самого тяжелого элемента группы наблюдается не только для Т1 в группе ШБ, но и для РЬ и Bi соответственно в IVB-и VB-группах. [3]
От металлов VB-группы они отличаются слабо выраженным свойством пассивироваться. Объясняется это летучестью оксидов молибдена и вольфрама при высоких температурах, вследствие чего невозможно образование защитных оксидных пленок на поверхности этих металлов. [4]
Водород связывается этими металлами непрерывно ( нестехиометрически), причем получаются твердые растворы гидридов с металлами. Кроме того, металлы VB-группы ( особенно в порошкообразном состоянии) взаимодействуют с серой, фосфором, бором и кремнием. [5]
Так, ванадий образует непрерывные растворы в твердом состоянии с р-титаном, металлами подгруппы хрома, б-марганцем, а-железом; ниобий образует непрерывные твердые растворы с ( - модификациями всех металлов подгруппы титана, молибденом, вольфрамом и у-ураном; тантал ведет себя в этом отношении аналогично ниобию. Таким образом, все три металла VB-группы являются хорошими растворителями и сами хорошо растворяются в других переходных металлах. В тех случаях, когда сочетание металлохимических факторов не благоприятствует полной взаимной растворимости, при взаимодействии с d - элементами образуются ограниченные твердые растворы с широкими областями гомогенности. [6]
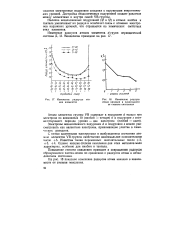 |
Изменение радиусов атомов элементов.| Изменение радиуса. [7] |
Иваются электронные подуровни соседних с наружными энергетических уровней. Достройка незаконченных подуровней создает различие между элементами и внутри самой VB-группы. [8]
Иодидный способ основан на том, что пары иодидов очищаемых металлов, устойчивые при низких температурах, разлагаются при соприкосновении с поверхностью сильно нагретой проволоки и чистый металл оседает на ее поверхности. Иодидным методом очищают от примесей титан, цирконий, металлы VB-группы. Например, очищаемый порошкообразный титан нагревают до 100 - 200 С с кристаллическим иодом в специальном аппарате. Сначала титан образует с иодом ( но не с примесями) летучий тетраиодид ТП4, пары которого затем разлагаются на поверхности накаленных электрическим током до 1300 - 1500 С тугоплавких нитей. Очищенный титан оседает на них, а освобождающийся иод образует новые порции тетраиодида титана, что обеспечивает непрерывность процесса очистки. [9]
Переход от ванадия к ниобию сопровождается весьма существенным изменением в химических свойствах соединений этих элементов. Так, в ряду амфотерных оксидов V2Os - Nb2Os - Ta2Os кислотные свойства резко уменьшаются от ванадия к ниобию. Как и следовало ожидать, кислотные свойства оксидов VB-группы выражены сильнее, чем у элементов IVB-группы: если ТК2 взаимодействует с гидроксидами щелочных металлов только в расплавах, то VO2 и V20s реагируют и с их растворами. [10]
Страницы: 1