Сульфид - литий
Cтраница 1
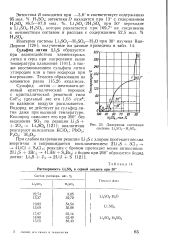 |
Растворимость Li2S04 в серной кислоте при 30. [1] |
Сульфид лития Li2S образуется при взаимодействии элементарных лития и серы при нагревании выше температуры плавления 1101 ], а также восстановлением сульфата лития углеродом или в токе водорода при нагревании. Теплота образования из элементов равна 115 26 ккал / моль. [2]
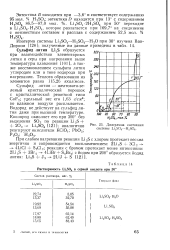 |
Растворимость Li2S04 в серной кислоте при 30. [3] |
Сульфид лития - желтовато-зеленый кристаллический порошок с кристаллической решеткой типа CaF2; удельный вес его 1 63 г / см3; во влажном воздухе расплывается. Водород не действует на сульфид лития даже при высокой температуре. [4]
Сульфид лития получают пои восстановлении Li2SO4 водородом или углеродом при нагревании. Полисульфиды лития-неустойчивые соединения и получают их в определенных условиях. Сульфид лития гигроскопичен, очень хорошо растворяется в воде, этаноле, хорошо - в разбавленной азотной кислоте и галоидоводородных кислотах, при этом образуются гидроокись, нитрат л галогениды лития соответственно. [5]
Сульфид лития, Li2S, образуется при реакции паров серы с расплавленным металлическим литием или же путем восстановления сульфата лития углеродом при нагревании. [6]
Сульфид лития получают в той же ловушке, где затем проводят взаимодействие с ОеНзВг. Ловушку подсоединяют к высоковакуумной аппаратуре через кран, смазанный фторсодержащей смазкой; все краны аппаратуры также должны быть смазаны. В ловушку помещают 39 мг лития и 93 мг серы, систему вакуумируют и при - 196 С конденсируют на реагенты 10 мл аммиака. Затем ловушку нагревают до - 64 С, встряхивая ее содержимое. После того как при этой температуре приблизительно через 1 ч исчезнет голубая окраска растворенного лития, аммиак отгоняют, а осадок оставляют еще на 2 ч в вакууме для того, чтобы удалить последние остатки аммиака. Следует обратить внимание на то, что ОеНзВг не осаждается в виде твердого вещества на стенках, а растворяется. В конце синтеза продукт фракционируют в высоком вакууме, используя три охлажденные до - 23, - 64 и - 96 С ловушки. В ловушке при - 64 С находится ( GeHshS. [7]
Сульфид лития представляет собой белый бесцветный порошок или бесцветные кубические кристаллы с плотностью 1 70 г / см3, плавящиеся при 900 - 975, очень плохо растворимые в воде. [8]
Сульфид лития гигроскопичен, расплывается во влажном воздухе. [9]
 |
Давление паров щелочных металлов в зависимости от.| Скорость испарения щелочных металлов в зависимости от температуры. [10] |
Сульфид лития LLS получают действием паров серы на нагретый литий. [11]
Кислый сульфид лития ( гидросульфид) можно получить, действуя сероводородом на нагретый до красного каления карбонат лития или на металлический литий в эфире. Это соединение белого цвета, очень гигроскопично, растворимо в воде и этиловом спирте. [12]
При нагревании сульфида лития с углем в электрической печи образуется карбид лития Li2S - f - 2C - Li2C2 S. Фосфор при нагревании до 1000 не реагирует с сульфидом; хлорид мышьяка разлагает его с образованием сульфида мышьяка. [13]
Водород не действует на сульфид лития даже при высокой температуре. [14]
Литий и сера Аморфный сульфид лития LiaS был приготовлен действием паров серы на нагретый литий. [15]
Страницы: 1 2