Атомный азот
Cтраница 2
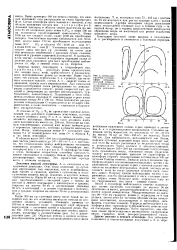 |
Схема циркуляции в гстеро-ефоре ( меридиональный разрез. а - в период со. тш - Ш Стсишил. ( J - в период равноденствия. [16] |
В отличие от О2, у N2 не происходит сильной диссоциации иод действием солнечного излучения, поэтому в целом атомного азота N в А. Максимум слоя атомного азота днем находится на высоте ок. Несмотря на низкую концентрацию, атомный азот играет важную роль в аурономич. N составляет примерно 0 1 от концентрации осн. [17]
Получение атомного азота может быть осуществлено путем пропускания газоооразного N2 ( под сильно уменьшенным давлением) сквозь поле высокочастотного электрического разряда. Так как энергии активации реакций с участием свободных атомов обычно весьма малы ( часто - близки к нулю), атомный азот гораздо активнее молекулярного: уже при обычной температуре он непосредственно соединяется с S, P, As, а также с Hg и рядом других металлов. [18]
 |
Разорванный участок трубы змеевика печи риформинга. [19] |
Впервые разрушения печных труб от действия азота на сталь были обнаружены на установках, где создались условия для диссоциации аммиака на водород и азот. Этот процесс протекает при температурах выше 400 С, а при температурах более 600 С молекулярный азот диссоциирует с образованием активного атомного азота, который диффундирует вглубь стали и вызывает разупрочнение ее структуры. С этим явлением пришлось столкнуться при изучении работы ядерных реакторов, где отвод тепла осуществляется током чистого азота. Особенно активно реагируют с ним нержавеющие стали, содержащие хром, алюминий, титан и другие легирующие элементы. [20]
В отличие от О2, у N2 не происходит сильной диссоциации иод действием солнечного излучения, поэтому в целом атомного азота N в А. Максимум слоя атомного азота днем находится на высоте ок. Несмотря на низкую концентрацию, атомный азот играет важную роль в аурономич. N составляет примерно 0 1 от концентрации осн. [21]
Те же Бей и Штейнер - недавно показали, что метастабильные молекулы, образованные в разряде, могут быть выведены из зоны разряда. Этим самым было дано доказательство тому, что рекомбинация атомов азота не является единственным способом образования метастабильных молекул в послеразрядной зоне. В колебательном или конденсированном разряде образуется большое количество атомного азота. Вычислено, что при наиболее благоприятных условиях получается приблизительно 40 % атомов. [22]
Кистяковский 7, пользуясь видоизменением того же аппарата, исследовал потенциалы ионизации азота и водорода на железе и других металлах. Он пришел к выводу, что положительная ионизация, наблюдающаяся на железе, меди и платине при 11 и 13 V, принадлежит соответственно адсорбированному азоту и водороду. Кроме того он нашел, что 11-вольтный потенциал для азота относится к возбужденным молекулам азота или атомному азоту, скорее всего к последнему. Впрочем, судя по другим экспериментальным исследованиям адсорбированных газов на металлических поверхностях, кажется невероятным, чтобы азот, адсорбируясь в атомном состоянии, мог сохранять в этом виде свойства газообразного состояния. [23]
 |
Разрушенный участок трубы змеевика печи риформинга. [24] |
Впервые разрушения печных труб от действия азота на сталь были обнаружены на установках, где создались условия для диссоциации аммиака на водород и азот. Этот процесс протекает при температурах выше 400 С, а при температурах более 600 С молекулярный азот диссоциирует с образованием активного атомного азота, который диффундирует вглубь стали и вызывает разупрочнение ее структуры. С этим явлением пришлось столкнуться при изучении работы ядерных реакторов, где отвод тепла осуществляется током чистого азота. Особенно активно реагируют с ним нержавеющие стали, содержащие хром, алюминий, титан и другие легирующие элементы. [25]
Этот оксид окисляет SO2 до SO, на этой реакции основан нитрозный метод получения серной кислоты. Раздражает дыхательные пути, при больших концентрациях появляется отек легких. Для азотирования нагревают детали при 480 - 650 С в атмосфере аммиака, при этом образуется атомный азот, который поглощается поверхностью стальных деталей с образованием нитридов железа и нитридов легирующих элементов. Азотистая кислота HNO2 - слабая одноосновная кислота, существует только в разбавленных водных растворах. [26]
В течение многих лет было известно, что активный азот получается в результате электрического разряда в атмосфере азота. Этот газ имеет устойчивый золотисто-желтый цвет и химически очень активен. Они рекомбинируют сравнительно медленно, образуя возбужденные молекулы N. Большое различие в электронном спине, когда два атома в спиновых квартетных состояниях ( всего шесть неспаренных электронов) объединяются с образованием молекулы в квинтетном состоянии ( четыре неспаренных электрона) объясняет медленность рекомбинации, в то время как присутствие атомного азота объясняет высокую химическую активность. [27]
В течение многих лет было известно, что активный азот получается в результате электрического разряда в атмосфере азота. Этот газ имеет устойчивый золотисто-желтый цвет и химически очень активен. Они рекомбинируют сравнительно медленно, образуя возбужденные молекулы N, в квинтетных спиновых состояниях, которые затем испускают характерное излучение при переходе в основное состояние. Большое различие в электронном спине, когда два атома в спиновых квартетных состояниях ( всего шесть неспаренных электронов) объединяются с образованием молекулы в квинтетном состоянии ( четыре неспаренных электрона) объясняет медленность рекомбинации, в то время как присутствие атомного азота объясняет высокую химическую активность. [28]
Страницы: 1 2