Активность - вода
Cтраница 1
Активность воды имеет значение при комплексообразовании в смешанных растворах и концентрированных растворах электролитов, когда Н2О активность воды может заметно изменяться. В разбавленных растворах Н20 1 и количество параметров уменьшается до трех. [1]
Активность воды в растворах двух или большего числа электролитов может быть вычислена по данным для бинарных систем на основании правила Зданов-ского, согласно которому при смешении изопиестических растворов разных электролитов активность воды не изменяется. [2]
Активность воды определялась экспериментально и lgye / выражался как функция / и а. [3]
 |
Графическое определение.| Графическое определение состава изопиестических растворов в системе из трех солей и воды. [4] |
Активность воды в растворах, содержащих три и более солей, также может быть найдена графическим путем. Для этого строят диаграмму изоактиват для какой-либо пары солей. На оси ординат вниз откладывают точки, соответствующие концентрациям третьей соли при выбранных активностях воды, и, соединив их с соответствующими точками на оси абсцисс, получают диаграмму изоактиват для тройных растворов с постоянным отношением концентраций двух солей. [5]
Активность воды в растворах серной кислоты ( при концентрациях, имеющих место в свинцовом аккумуляторе) изменяется приблизительно в 1 5 раза, в то время как активность серной кислоты в том же интервале концентраций изменяется приблизительно в 20 раз. [6]
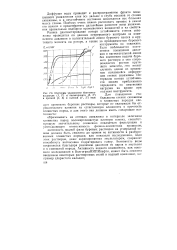 |
Изотермы увлажнения бентонита-аскангеля ( 1, 1 и палыгорскита ( 2, 2 в пресной ( /, 2 и соленой ( 1 2 воде. [7] |
Активность воды сохраняется благодаря различию давления ее паров в эмульсии и в глинистой породе. [8]
Активность воды сохраняется благодаря различию давления ее паров в эмульсии и глинистой породе. [9]
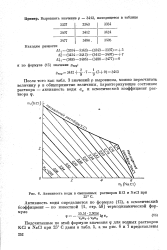 |
Активность воды в смешанных растворах КС1 и NaCl при. [10] |
Активность воды определяется по формуле ( 12), а осмотический коэффициент - по известной [ 1, стр. [11]
Активность воды в растворах двух или большего числа электролитов может быть вычислена по данным для бинарных систем на основании правила Зданов-CKOFO, согласно которому при смешении изопиестических растворов разных электролитов активность воды не изменяется. [12]
Активность воды в водных растворах равна р / р ( где р и р - давление водяного пара в равновесии с раствором и с чистой водой, соответственно) при данной температуре и условии, что р и р так низки, что водяной пар можно рассматривать как идеальный газ. [13]
Активность воды в процессе реакции практически не изменяется ( то же относится к чистым металлам и другим твердым веществам) и поэтому ее значение в уравнение не вводится. [14]
Активность воды при взаимодействии с силикатами и карбонатами значительно возрастает в присутствии углекислоты. Последняя, как подчеркивал В. Р. Вильяме ( 1936), играет главную роль в химическом выветривании горных пород. [15]
Страницы: 1 2 3 4