N-метилформамида
Cтраница 1
N-метилформамида уменьшается, что указывает на частичную десорбцию органических молекул с поверхности ртути. Этот результат может быть объяснен уменьшением эффективной диэлектрической проницаемости в двойном электрическом слое при вхождении в него молекул формамида или N-метилформамида. Таким образом, как это впервые было отмечено Фрумкиным [68], не существует простой зависимости между эффективной диэлектрической проницаемостью в двойном слое и макроскопической диэлектрической проницаемостью растворителя. [1]
При хранении N-метилформамид разлагается. [2]
N-метилацетамиде или N-метилформамиде изобразить в виде функции от ДЯ в пропиленкарбонате, то значения для солей катионов М4 и R N укладываются на одну прямую [ ср. [3]
Специфическая адсорбция катиона ( C g N из N-метилформамида, как сообщали Дамаскин и Поваров [9], значительно слабее, чем из водного раствора. Это было отнесено за счет более сильной адсорбции растворителя в растворах N-метилформамида. Однако более важным фактором, вероятно, является более сильная сольватация иона в N-метилформамиде. Максимальное понижение емкости происходит в области горба, так как, согласно теории переориентации диполей, объясняющей появление горба, растворитель может менее прочно удерживаться в этой области. [4]
Кривая Быстрова, которая частично основывается на величине / NO для N-метилформамида, хорошо описывает полученную величину. [5]
Дихлоризомасляная кислота легко получается прямым хлорированием алкилметакрилатов в присутствии диметилформ-амида, N-метилацетамида, N-метилформамида, метакриламида или других подобных катализаторов, с последующим гидролизом образующегося эфира дихлоризомасляной кислоты водными растворами едких щелочей при температуре ниже 40 С. [6]
С при давлении 1 мм) и дважды без P2Os - При хранении N-метилформамид разлагается. [7]
Судя по относительному понижению пограничного натяжения ( табл. 3), адсорбция анионов из N-метилформамида сильнее, чем из формамида, хотя все еще значительно слабее, чем из воды. [8]
Специфическая адсорбция ионов Cs, по-видимому, происходит сильнее из диметилформамида, чем из формамида и N-метилформамида. CsCl ( при - 1 6 В относительно водного НКЭ), сообщенного Дамаскиным и Ивановой [7] для N-метилформамида. Это подтверждается измерениями емкости [46] для растворов Csl ( рис. 22), где обнаруживаются резкое возрастание емкости и сильная концентрационная зависимость в катодной области. Кривые для LiCl ( рис. 23), напротив, совершенно плоские и почти не зависят от концентрации. [9]
В этом разделе будут рассмотрены работы, которые привели к установлению шкал стандартных потенциалов в ацетонитриле, формамиде, N-метилформамиде и расплавленном хлориде ди-метиламмония. [10]
Предположение о специфических взаимодействиях между я-электронами бензольного кольца и частичными положительными зарядами в молекуле подтверждается результатами, полученными [10] для N-метилформамида III. В спектре N-метил-формамида имеются два вида резонансных сигналов, каждый из которых соответствует конфигурациям III и IV относительно пептидной связи. [11]
Однако электрокапиллярные измерения, выполненные Безуг-лым и Коршиковым [3, 4], показывают, что диметилформамид - интересный растворитель по отношению и к формамиду, и к N-метилформамиду, а также к воде. [12]
При 20 С измерены кривые дифференциальной емкости, электрокапиллярные кривые, величины поверхностного натяжения на границе раствор / воздух, а также эквивалентные электропроводности и вязкости для растворов LiNO3 н формамиде, N-метилформамиде и диметилформамиде в интервале концентраций от О, N до насыщенного. На основе полученных данных установлено, что строение двойного электрического слоя на границе между ртутью и концентрированными растворами LiNO3 в этих растворителях может быть интерпретировано в рамках предположения о сильной сольватации ионов Ц и NO при наличии сил зеркального изображения, уменьшающих толщину диэлектрической прослойки между поверхностью электрода и ионной обкладкой двойного слоя. [13]
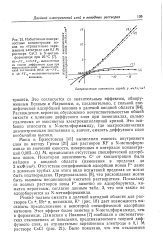 |
Избыточные поверхностные концентрации ионов на отрицательно заряженном электроде для 0 1 М раствора CsCl в N-метил-формамиде при 25 С. [14] |
Расхождение, вероятно, обусловлено нечувствительностью общей емкости к влиянию диффузного слоя при потенциалах, сильно удаленных от максимума электрокапиллярной кривой. Это особенно относится к N-метилформамиду, где макроскопическая диэлектрическая постоянная и, значит, емкость диффузного слоя необычайно высоки. [15]
Страницы: 1 2