Количество - металлическое железо
Cтраница 2
 |
Прибор для получения FeS. [16] |
Хрупкая сероватая кристаллическая масса ( моноклинной системы), легко растирающаяся в зеленовато-серый порошок. Легко растворяется в кислотах ( с выделением H2S), если содержит некоторое количество свободного металлического железа. На этом основан лабораторный метод получения сероводорода; водород, содержащийся в качестве примеси к HaS, не мешает для аналитических работ. [17]
 |
Прибор для получения FeS. [18] |
Хрупкая сероватая кристаллическая масса ( моноклинной системы), легко растирающаяся в зеленовато-серый порошок. Легко растворяется в кислотах ( с выделением HZS), если содержит некоторое количество свободного металлического железа. На этом основан лабораторный метод получения сероводорода; водород, содержащийся в качестве примеси к H2S, не мешает для аналитических работ. [19]
Получение высокотитаннстых шлаков состоит из восстановления исходного сырья ( титаномагне-титов) углеродом и электроплавки восстановленного продукта с целью разделения чугуна и шлака, поэтому последний всегда содержит некоторое количество металлического железа. [20]
Один из вариантов этого метода заключается в обработке пробы раствором хлорной ртути и салицилата натрия в метиловом спирте. При этом металлическое железо переходит в раствор, окисляется до Fe ( III) и связывается в салицилатный комплекс. Количество металлического железа определяют по интенсивности окраски образовавшегося салицилатного комплекса железа в присутствии ацетатного буферного раствора. Присутствие в растворе ртути, салицилата и метилового спирта не мешает определению. [21]
Сравнение этих результатов с данными Хербста и Халле [19] и Гофера [20, 21] показывает, что карбид с точкой Кюри 260 - 265 являлся Fe2C ( Хэгга), а карбид с точкой Кюри 380 являлся Fe2G с гексагональной решеткой. Отдельные порции этого обуглероженного катализатора нагревали в течение 30 мин. Нагревание при 300 ( рис. 117, В) привело лишь к незначительному изменению термомагнитной кривой; было установлено присутствие некоторого количества металлического железа. [22]
Определение содержания металлического железа основано на взаимодействии его с ионами металла, имеющего более высокий электродный потенциал. С этой целью навеску губчатого железа обрабатывают [170] нейтральным раствором сернокислой меди. Металличеркое железо при этом переходит в раствор в двухвалентной форме, а медь выделяется в элементарном состоянии эквивалентно перешедшему в раствор железу. Количество металлического железа устанавливают путем определения двухвалентного железа в растворе перманганатным методом. Окислы железа при этой обработке остаются без изменения. [23]
Немагнитная область на рис. 8 получена на основании данных термомагнитного анализа преимущественно в относительно малых магнитных полях, однако эту оценку количеств металлического железа, карбида Хэгга и магнетита можно считать приблизительно правильной. В этом испытании на поверхности отлагалось лишь небольшое количество элементарного углерода; дезактивация и потеря механической прочности катализатора в основном должны быть отнесены за счет окисления, а не за счет образования свободного углерода. [24]
Сравнение этих результатов с данными Хербста и Халле [19] и Гофера [20, 21] показывает, что карбид с точкой Кюри 260 - 265 являлся Fe2C ( Хэгга), а карбид с точкой Кюри 380 являлся Fe2G с гексагональной решеткой. Отдельные порции этого обуглероженного катализатора нагревали в течение 30 мин. Нагревание при 300 ( рис. 117, В) привело лишь к незначительному изменению термомагнитной кривой; было установлено присутствие некоторого количества металлического железа. После нагревания при 480 точка Кюри 380 исчезла и количество металлического железа возросло. Очевидно, это соответствует смеси цементита и Fe2C ( Хэгга); магнитные весы были, вероятно, недостаточно чувствительны для того, чтобы показать обе близко-лежащие точки Кюри. [25]
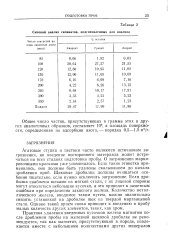 |
Ситовой анализ силикатов, подготовленных для анализа. [26] |
Агатовые ступки и пестики часто являются источником загрязнения, но введение постороннего материала может встречаться на всех стадиях подготовки пробы. Если такие этикетки применялись, они должны быть удалены скалыванием до начала дробления проб. Щековые дробилки должны очищаться особенно тщательно, если нужно исключить загрязнение. Если дробилка снабжена щеками из мягкой стали, с их лицевой стороны могут отколоться небольшие кусочки, а это приводит к заметным ошибкам при определении закиспого железа. Количество металлического железа, вводимое таким путем, можно значительно снизить установкой на дробилке щек из твердой марганцевой стали. Однако такой прием снова приводит к введению в пробу малых количеств других элементов, таких, как хром. [27]
Такому условию удовлетворяют порошки из металлов и ферросплавов, активно сгорающих в струе кислорода с образованием жидких шлаков. Вводимые порошки выполняют двойную роль. С одной стороны, порошок, воспламеняясь и сгорая на разрезаемой поверхности, значительно повышает температуру зоны реза. С другой стороны, продукты окисления, сплавляясь с окислами поверхностной пленки, образуют шлаки с более низкой температурой плавления, легче поддающиеся удалению из разреза. Однако длительные испытания различных порошковых композиций показали, что наиболее рациональным является использование в качестве флюса мелкогранулированного железного порошка. Железый порошок при сгорании выделяет большое количество тепла ( около 1800 ккал / кг), не образует тугоплавких окислов, а продукты окисления железа ( распыленные окислы железа и некоторое количество металлического железа) не ядовиты. Кроме того, продукты окисления железного порошка, сплавляясь с окислами поверхностной пленки, образуют шлаки с более низкой температурой плавления, легче поддающиеся удалению из зоны реза. [28]
Страницы: 1 2