Данный компонент
Cтраница 3
Самопроизвольный переход данного компонента возможен из фазы, для которой его химический потенциал больше, в фазу, где он меньше, до выравнивания их значений в обеих фазах. [31]
Переход массы данного компонента между фазами происходит только при различии в значениях химического потенциала этого компонента. Если все его потенциалы равны между собой, то между фазами существует равновесие. Давление, температура и состав фаз при равновесии являются основными параметрами для анализа процессов испарения. Рассмотрение различных типов равновесия, в частности, встречающихся при перегонке, составляет содержание этой главы. Самые процессы перегонки будут рассмотрены в следующей главе. [32]
Химические потенциалы данного компонента во всех фазах системы, находящейся в равновесии, равны между собой. Если химические потенциалы данного компонента в разных фазах системы различны, то самопроизвольно компонент переходит из фазы, где химический потенциал больше, в фазу, в которой он меньше. Переход продолжается до тех пор, пока химические потенциалы компонента в обеих фазах не сравняются. [33]
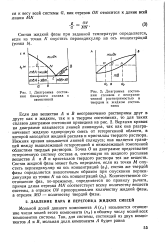 |
Диаграмма состояния бинарного сплава с эвтектикой.| Диаграмма состояния сплавов с неограниченной растворимостью в твердом и жидком состояниях. [34] |
Мольной долей данного компонента А ( ХА) называется отношение числа молей этого компонента ( ПА) к общему числу молей всех компонентов системы. [35]
Аллотропические изменения данного компонента в двухфазной области происходят при постоянной температуре, и на диаграмме состояния этому изменению будет соответствовать линия, параллельная оси состава. [36]
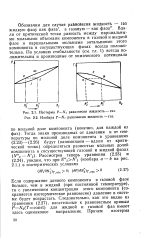 |
Изотерма Р - Ni равновесия жидкость - газ. [ IMAGE ] Изобара Т - Ni равновесия жидкость - газ. [37] |
Если содержание данного компонента в газовой фазе больше, чем в жидкой ( при постоянной температуре), то с увеличением концентрации этого компонента ( сохраняется изотермическое равновесие) давление в системе будет возрастать. Следовательно, как это видно из уравнения (2.27), касательные к равновесным кривым Я - 2 ( Т const) для жидкой и газовой фаз имеют здесь одинаковое направление. [38]
Коэффициент активности данного компонента ( так же, как и его активность) характеризует степень отклонения свойств компонента в растворе от его свойств в соответствующем идеальном растворе. [39]
Мольная доля данного компонента равна отношению числа его молей к общему числу молей всей смеси. [40]
Весовой концентрацией данного компонента называется отношение веса его в чистом виде к весу всего раствора. [41]
Весовым содержанием данного компонента называют отношение веса его к весу другого компонента в растворе. [42]
Преимущественная конденсация данного компонента на этом этапе позволяет получить обогащенную им уловленную пыль. [43]
Мольная доля данного компонента в парах, поднимающихся из кипятильника, Уи - Kwxw, где xw - его мольная доля в жидкости, находящейся в кипятильнике, и Да, - константа фазового равновесия, соответствующая температуре кипения жидкости в кипятильнике. [44]
Мольная доля данного компонента в парах, поднимающихся из кипятильника, Уа Kwxw, где xw - его мольная доля в жидкости, находящейся в кипятильнике, и АИ, - константа фазового равновесия, соответствующая температуре кипения жидкости в кипятильнике. [45]
Страницы: 1 2 3 4