Конверсия - нитрат - кальций
Cтраница 1
Конверсия нитрата кальция осуществляется методом обмен -) го разложения. [1]
Способ получения натриевой селитры конверсией нитрата кальция и природного сульфата натрия является одной из попыток заменить дефицитное и сравнительно дорогое сырье - Кальцинированную соду - природным сульфатом натрия. Последнего имеются в СССР значительные запасы, и поэтому положительное разрешение вопроса может дать возможность сельскому хозяйству получить в большом количестве дешевую натриевую селитру. [2]
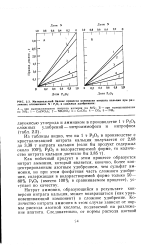 |
Материальный баланс процесса конверсии нитрата кальция при различных отношениях N. Р2О5 в сложных удобрениях. [3] |
Нитрат аммония, образующийся в результате конверсии нитрата кальция, может возвращаться ( как уравновешивающий компонент) в сложное удобрение. Количество нитрата аммония в этом случае зависит от нормы расхода азотной кислоты, подаваемой на разложение апатита. [4]
При использовании неполной нормы сульфата аммония для конверсии нитрата кальция, а именно 3 5 моля ( NH4) 2SO4 на 1 моль апатита, затраты на переработку 1 т апатитового концентрата разложением его неполной нормой азотной кислоты меньше на 25 - 30 %, чем затраты на получение нитрофоски, содержащей всю P2Os в водорастворимой форме по обычному сульфатному способу. Эти затраты также ниже на-20 % по сравнению даже с затратами на получение частично воДораствори - мой нитрофоски по обычному сульфатному способу. [5]
В перспективе возрастет количество нитрата аммония, получаемого конверсией нитрата кальция, который образуется при азотнокислотной переработке фосфатов ( см. гл. [6]
 |
Расходные нормы на 1 т суммы действующих веществ. [7] |
Производство нитрофоски азотнокислотным способом с политермической кристаллизацией и конверсией нитрата кальция отличается наименьшей стоимостью сырья по сравнению с другими способами получения этого продукта. [8]
 |
Схема процесса переработки азотнофосфорнокислотного раствора. [9] |
I: I в сатураторы дополнительно вводят раствор NH4NO3, получаемый со стадии очистки газовых выбросов и конверсии нитрата кальция. Раствор аммонизируют газообразным аммиаком, подаваемым в сатураторы через бар-ботеры. За счет тепла химической реакции температура в процессе аммо-низации достигает 125 С. При этом 30 - 35 % воды, поступающей на ам-монизацию вместе с азотнофосфорнокислотным раствором, испаряется. [10]
На установке, описанной в предыдущем параграфе ( см. рис. VIII-3), были проведены опыты по газовой конверсии нитрата кальция в карбонат кальция и нитрат аммония. Реактор 11 дополнительно был оборудован электрообогревом. [11]
На рис. VIII-27 представлена технологическая схема производства нитрофоски с разложением фосфата азотной кислотой и политермической кристаллизацией и конверсией нитрата кальция. После осветления азотнофосфорнокислого раствора и кристаллизации тетрагидрата нитрата кальция последний отделяется и промывается азотной кислотой и водой на фильтре. Маточный раствор нейтрализуется аммиаком в нейтрализаторах, в которые для поддержания заданного соотношения N: Р О вводится также часть раствора нитрата аммония, образующегося в результате конверсии нитрата кальция. [12]
 |
Расходные коэффициенты на 1 т суммы питательных веществ ( N - - PsOb - - KzO в производстве сложных удобрений азотнокислотным способом. [13] |
При сопоставлении технико-экономических показателей раз личных способов переработки азотнокислотного раствора оче -; видно преимущество схемы получении нитроаммофоски с вымораживанием и конверсией нитрата кальция. [14]
Показанные на графике расходы азотной кислоты и аммиака на получение нитрофосфатов учтены только в той доле, в какой они остаются ( или возвращаются после конверсии нитрата кальция в нитрат аммония) в готовом удобрении. Для выведенного из реакции нитрата кальция, применяемого в дальнейшем как самостоятельный продукт, требуется дополнительное количество азотной кислоты. [15]
Страницы: 1 2