Конденсация - нитрил
Cтраница 1
Конденсация нитрилов с альдегидами в присутствии серной кислоты проводится при комнатной температуре или при нагревании до температуры 30 - 50 С. Для получения бис-амйдов серную кислоту обычно добавляют к смеси нитрила и альдегида. [1]
Конденсация нитрилов с а л к и л нитр а т а м и. Первичные нитросоединения можно получать из нитрилов, имеющих метиленовую группу рядом с нитрильной группой, конденсацией с эфирами азотной кислоты под действием этилата натрия ( Вислииенус. [2]
Конденсация нитрилов с алкилнитратамн. [3]
При конденсации нитрилов а-кетокислот с замещенным аминогуанидином в органическом растворителе в присутствии кислотного катализатора получают 3 4-дизамещенные - 5-имиио - 1 2 4-триазины. [4]
Многочисленные исследования реакции конденсации нитрилов с резорцином, флороглюцином и их эфирами показали, что эта реакция очень удобна для получений полиоксикетонов. Выходы кетонов из флороглюцина или его эфиров и алифатических нитрилов превышают 70 % ( за исключением нитрилов очень сложного строения); резорцин и его эфиры дают обычно более низкие выходы. Ароматические нитрилы реагируют не так легко, как алифатические. [5]
В качестве агента, вызывающего конденсацию нитрилов с альдегидами, наиболее часто используется концентрированная серная кислота. При получении бис-амида из фенил-ацетонитрила и бензальдегида в присутствии серной кислоты в растворе уксусной кислоты было найдено9, что существует оптимальное содержание серной кислоты ( около 0 2 моль на 1 моль нитрила), выше которого выход бис-амида снижается из-за протекания побочной реакции гидратации нитрила, приводящей к образованию фенилацетамида. [6]
Первоначальный вариант процесса Торпа включал межмолекулярную катализуемую основаниями конденсацию нитрилов; позднее Торп разработал внутримолекулярный процесс, используя сс. Эта реакция пригодна для получения циклоалканов, поскольку первоначальный продукт - енаминонитрил - гидролизу-ется и декарбоксилируется в кислой среде. Циглер показал, что после модификации реакция Торпа может быть использована для синтеза циклических кетонов, содержащих от 5 до 33 атомов углерода. [7]
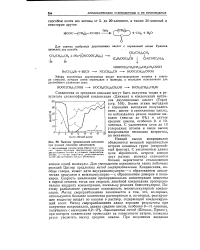 |
Выходы производных цикланов при разных способах циклизации. [8] |
Соединения со средними циклами могут быть получены также в результате сложноэфирной конденсации ( Дикман) и конденсации нитрилов двухосновных кислот ( Торп) ( стр. [9]
Дигидро-1 3 4-тиадиазины получают действием пентасульфида фосфора на Л / - ацил - ЛГ - ( р-гидро-ксиалкил) - Л / - метилгидразины и конденсацией нитрилов, имидатов, бромистого циана или этилортоформиата с 1-метил - 1 - ( р-меркап-топропил) гидразином. Последнее соединение при взаимодействии с бензальдегидом превращается в тетрагидро-1 3 4-тиадиазиновое производное. [10]
Для получения больших и средних циклов можно применять те же общие методы, что и для синтеза пяти - и шестичленных циклов, а именно: пиролиз двухосновных кислот над ТЬ02, конденсацию нитрилов и особенно ацилоиновую конденсацию. Многие макроциклические соединения впервые были синтезированы Ружичкой прокаливанием ториевых солей двухосновных кислот в вакууме. [11]
Аллилалкилкетоны легко изомеризуются в пропенильные изомеры при нагревании с разбавленной серной кислотой. Вследствие этого, при получении ( 3 у-непредельных кетонов путем конденсации нитрилов с йодистым аллилом и цинком, необходимо тщательно избегать разогревания при разложении цинкорганического комплекса водой и серной кислотой. [12]
Таким образом было получено много различных кетиминов. Они представляют собою основные бесцветные сильнопреломляющие свет жидкости или низкоплавкие твердые тела несколько неприятного запаха. Многие кетимины, особенно жирно-ароматических кетонов, образуются в качестве промежуточных продуктов при получении кетонов конденсацией нитрилов с ароматическими соединениями. [13]
Страницы: 1