Консден
Cтраница 3
После того как ХТС была; разработана Шталем [196-200] в виде простой и стандартной методики, с таким исключительным успехом использованной в первую очередь для разделения липофильных и гидрофильных веществ и превосходящей метод, хроматографии на бумаге, казалось соблазнительным распространить эту методику на метод ИТС. В принципе при осуществлении этой методики н & возникает трудностей; Консден, Гордон и Мартин [99] уже в 1946 г. успешно применили силикагель в качестве носителя для разделения аминокислот и пептидов методом ионофореза. [31]
Решение общего уравнения является слишком сложным. Поэтому в дальнейшем мы возьмем упрощенное выражение, при выводе которого использованы те же допущения, что и у Мартина и Синга и у Консдена с сотрудниками. [32]
Стремясь избежать подобного рола объективных ошибок, мы обратились к ряду ученых, занимавшихся определением аминокислотного состава белков, с просьбой предоставить соответствуют:; ; матлзнал. Кроме того, мы сочли целесообразным привести перечень литературы, в которой можно найти интересующие читателя сведения по аминокислотному составу белков, полученные в СССР. Консден, Еердон и Мартин, Biochem. По не зависящим от редактора и переводчика обстоятельствам именной и предметный указателя не охватывают примечании и библиографии, помещенных ниже в тексте. [33]
Аналогичную картину развития мы наблюдаем, и в случае колоночной хроматографии Цвета ( рис. 2); прошло свыше 20 лет, пока работдми Рихарда Куна не было доказано значение этого метода. Лишь полвека спустя Консден, Гордон, Мартин и Синдж создали из этого полезный метод. [34]
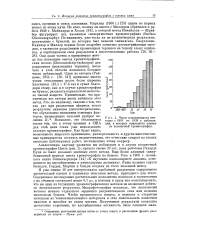 |
Число появляющихся ежегодно с 1903 по 1938 г. публикаций, в которых приводятся данные по колоночной хроматографии. [35] |
Аналогичную картину развития мы наблюдаем и в случае колоночной хроматографии Цвета ( рис. 2); прошло свыше 20 лет, пока работами Рихарда Куна не было доказано значение этого метода. Лишь полвека спустя Консден, Гордон, Мартин и Синдж создали из этого полезный метод. [36]
На разделении аминокислот неблагоприятно сказывались адсорбционные свойства используемого инертного носителя, чаще всего силикагеля. В 1943 г. Мартин, Консден и Гордон использовали для анализа малых количеств аминокислот фильтровальную бумагу в качестве носителя неподвижной водной фазы, а в качестве подвижной фазы смесь органического растворителя с водой. [37]
Мартин и Спнг, применявшие сначала для разделения ацетиламинокислот экстракционный метод 11 ], решили закрепить одну из фаз на порошкообразном носителе. В качестве такого носителя сначала был выбран силпкагель. Последний добавляли для того, чтобы воспрепятствовать действию сшшкагеля как адсорбента, а также для повышения растворимости в подвижной фазе. Действие сшшкагеля как адсорбента и трудность стандартизации его приготовления оказывают неблагоприятное влияние на разделение при использовании силикагеля в качестве носителя. Консден, Гордон, Мартин и Сннг ( рис. 5), которые в то время проводили работы в Лидсе по исследованию шерсти, использовали для анализа малых количеств неацетилировашшх аминокислот фильтровальную бумагу. Таким образом, можно сказать, что распределительная хроматография на бумаге, появившаяся в 1943 г. благодаря работам Гордона с сотрудниками [1] и Кон-сдена с сотрудниками, имела три источника: хроматографию Цвета, противоточное распределение и частично капиллярный анализ. Различие между распределительной хроматографией на бумаге и капиллярным анализом уже было рассмотрено выше ( см. стр. [38]
Слегка влажная бумага имеет тенденцию сворачиваться, причем ось искривления бывает параллельна продольной оси. Неоднородность структуры бумаги может привести к неравномерной скорости протекания растворителя в разных направлениях и вследствие этого к плохой воспроизводимости результатов. Перемещение фронта растворителя ( границы между сухой и влажной бумагой) на нисходящей хроматограмме происходит более равномерно, чем на восходящей хроматограмме. Однако даже при нисходящем токе жидкости поведение растворителя вблизи резервуара жидкой фазы и у движущегося фронта неодинаково. В исходной части хроматограммы в процессе первоначального пропитывания растворитель протекает как по поверхности бумаги, так и сквозь пропитанную зону. Вблизи фронта растворителя жидкость просачивается вперед через тончайшие капилляры. Скорости передвижения растворенных веществ определяются относительными величинами распределения между подвижной жидкой фазой и стационарной гелеподобной фазой, которая, как принято считать, находится в аморфных участках целлюлозы. Хорошая бумага содержит не менее 96 % сс-целлюлозы ( нерастворимой в крепких растворах NaOH), около 40 % которой находится в аморфном состоянии. Консден, Гордон и Мартин [1] сопоставляли стационарную фазу с концентрированным раствором растворимого полисахарида. Скорости движения отдельных аминокислот приближаются к рассчитанным для простого распределения между двумя жидкими фазами, но ввиду сильного сродства основных аминокислот к целлюлозе, по-видимому, проявляются эффекты специфической адсорбции или ионного обмена. [39]
Страницы: 1 2 3