Константа - обмен
Cтраница 1
Константа обмена зависит от температуры и химической природы ( заряд и размер ионов, их гидратация) обменивающихся ионов и ионита. Она характеризует прочность закрепления данного иона в решетке ионита. Для многозарядных катионов константа обмена тем больше, чем выше заряд катиона, и возрастает с величиной порядкового номера элемента. [1]
Константа обмена fei 2 дает количественную характеристику адсорбируемости одного иона по сравнению с другим. При обмене одновалентных ионов nin2 в случае feul второй ион имеет большую адсорбируемость - реализуется выпуклая изотерма Ленгмюра, в случае fei al адсорбируемость обоих ионов одинакова - линейная изотерма Генри, в случае k t 1 - второй ион имеет меньшую адсорбируемость - вогнутая изотерма. [2]
Константа обмена соответствует минимуму свободной энергии и является мерой сродства обмениваемого иона к решетке обмен-ника при данной температуре. Константа обмена зависит также от химической природы обменивающихся ионов, их валентности и размеров в гидратированном состоянии. [3]
Константы обмена в неводных системах обычно приближаются к единице. Экспериментальные исследования показали, что константа обмена ионов окситетрациклина с ионами водорода на смоле СБС-3 в метиловом спирте падает до 10, а обратная ей константа обмена возрастает до 0.1. В соответствии с этим десорбция окси - и хлортетрациклина раствором НС1 в метаноле приводит к вытеснению всего антибиотика с довольно высокой концентрацией ( рис. 63, б; 64), так как в процессе десорбции размывание границы зон ионов протекает не очень сильно. Кроме того, сорб-ционный процесс необходимо проводить в колонках ограниченной высоты, так как размывание границы зон ионов может привести к снижению концентрации антибиотиков в элюате. Однако для последующей очистки антибиотиков использование этих растворителей менее желательно. [4]
Константа обмена дает количественную характеристику сорбции одного иона по сравнению с другим. [5]
Константа обмена позволяет количественно характеризовать равновесие ионного обмена. Статика ионообменного равновесия имеет большой теоретический и практический интерес. Предложено несколько эмпирических уравнений для описания статики ионного обмена. [6]
Константа обмена может рассматриваться, как средняя характеристика кислотных свойств стекла. Поэтому, по мере роста отношения [ B2O3 ] / [ Na2O ] константа К должна расти, что соответствует опыту. Это также соответствует опыту. [7]
Константа обмена К в уравнениях Никольского характеризует разницу в прочности связи Н и Ма - ионов в стекле и в растворе. [8]
Константа обмена может рассматриваться, как средняя характеристика кислотных свойств стекла. Поэтому, по мере роста отношения [ Bs03 ] / [ Na2O ] константа К должна расти, что соответствует опыту. Это также соответствует опыту. [9]
Константы обмена могут служить для характеристики сродства ионита к различным ионам. Но из-за трудностей в определении активностей ионов в смоле и растворе для представления сорбируемости ионов используют экспериментально определяемые коэффициенты распределения, которые равны отношению концентраций данного иона в равновесных фазах. [10]
Константа обмена будет возрастать и степень обмена ионов ( М - Н) - на анионы будет увеличиваться в тех случаях, когда Kayi КаН2О, и будет уменьшаться в тех случаях, когда Кам KailiQ. [11]
Константа обмена / С в уравнениях Никольского характеризует разницу в прочности связи Н и N а - ионов в стекле и в растворе. [12]
 |
Влияние значения рН на емкость битумных катионитов СБН ( 1 - 3 и СБТ. (. - 3 по ионам стронция ( 1, 1, цезия ( 2, 2 и натрия ( 3, 3. [13] |
Константы обмена одного металла на другой были определены косвенным методом из двух-компонентной системы металл-водород. При одновременном присутствии ионов двух металлов величины констант обмена, как указывалось ранее [8], изменяются ( особенно для полифункциональных ионитов), поэтому в реальных случаях коэффициенты разделения указанных пар ионов на битумных катионитах будут иметь, по-видимому, бблыпие значения. [14]
 |
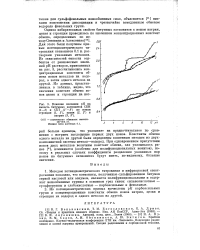
Теоретические кривые распределения иона, сорбируемого в динамических условиях при разных значениях ионного отношения и констант обмена. [15] |
Страницы: 1 2 3 4