Константа - равновесие - изомеризация
Cтраница 1
Константы равновесия изомеризации, как скелетной, так и: структурной, также слабо меняются с температурой ( для них малы не только теплоты, но и изменения энтропии), и это приводит к относительной стабильности состава равновесной смеси в довольно широком диапазоне температур. Таким образом, изомеризация; пипериленов в изопрен в проточном реакторе затронет не больше трети сырья и потребует значительной рециркуляции. Учитывая, что изомеризация скелета диенов сопровождается интенсивными побочными реакциями перераспределения водорода, представляется более целесообразным ( по технологическим, а не термодинамическим соображениям) превращать пиперилены в н-пентан или н-пентен, изомеризация которых реализуется в промышленности. В ряде работ, в том числе и нашей [39], предложены каталитические системы для гидрирования пипериленов. [1]
А, если известны все константы равновесия изомеризации. [2]
На рис. 4.20 представлена зависимость константы равновесия изомеризации кристаллического фиолетового в РММА и PC от давления. [3]
Принимая, что при 900 К константа равновесия изомеризации близка к 7, они получили хорошее согласие с эксперимент том. [4]
В заключение в табл. 58 приводим константы равновесия изомеризации 1-бутена, 1-пентена и 1-гексена в различные изомеры. Эти величины рассчитаны по данным, приведенным в табл. 9 - 10 ( см. стр. Справочника), Погрешности в константах равновесий гексенов, вероятно, довольно значительны. [5]
Состав равновесной смеси рассчитывается на основании констант равновесия изомеризации каждого углеводорода в один - стандартный. [6]
Следует отметить, что движущую силу вытеснения кислорода создает электронная пара на амине и наоборот, что константа равновесия изомеризации неполярного промежуточного соединения в биполярное может влиять на направление его распада, так что направление распада зависит не только от относительной легкости удаления возможных уходящих групп. [7]
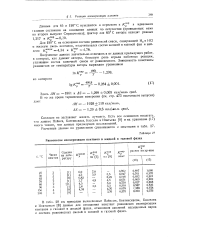 |
Равновесие изомеризации пентанов в жидкой и газовой фазах. [8] |
В табл. 28 мы приводим вычисленные Пайнсом, Кветинскасом, Касселем и Ипатьевым [8] данные для отношения констант равновесия изомеризации пентанов в газовой и жидкой фазах, отношения давлений насыщенных паров и составы равновесных смесей в жидкой и газовой фазах. [9]
На основании весьма точно определенных тепловых эффектов и расчетов по теореме Нернста и по спектроскопическим данным Россини, Про-зен и Питцер [15] вычислили константы равновесия изомеризации бутанов, пентанов, гексанов и гептанов. [10]
Следует иметь в виду, что экспериментальные данные, особенно относящиеся к высоким температурам, должны отличаться от расчетных несколько меньшим содержанием устойчивого изомера и соответственно большими концентрациями неустойчивых изомеров, так как энтропийные характеристики в данном случае более благоприятны для изомеров, термодинамически менее устойчивых. Расчет состава равновесной смеси проводится на основании констант равновесия изомеризации каждого углеводорода в один - обычно наиболее устойчивый. [11]
Как и к-бутан, циклогексан не имеет третичного атома водорода и не может быть эффективным ингибитором. Кроме того, скорость его изомеризации в метилциклопеятан, являющийся активным ингибитором, много ниже, чем скорость превращения 2 2 4-триметилпентана. Поскольку константа равновесия изомеризации метилциклопентана в циклогексан при 26 равна приблизительно восьми, то скорость изомеризации циклогексана должна приблизительно составлять J / se от скорости превращения 2 2 4-триметилпентана. Хотя подтверждающих это данных не имеется, весьма вероятно, что изомеризация циклогексана протекает быстрее, чем изомеризация и-пентана. Поэтому циклогексан действует как активный ингибитор при применении вместе с к-пентапом. [12]
Бьеллерап [137] измерял энтальпию сгорания и вычислил & HfM9 ( l) - 29 73 ккал / молъ и AHf 2ss ( g) - 21 98 ккал / молъ. Бьеллерап рассчитал также значение & Hf 2w ( g) - 21 77 ккал / молъ по энтальпии реакции между циклопропаном и бромистым водородом, установленной Лейчером, Кианпуром и Парком [829], а также значение А / 7 / 2Э5 ( g) - 21 15 ккал / молъ по энтальпии реакции между 1-бром-пропаном и водородом на основании неопубликованных данных, сообщенных Лейчером. Более ранние данные по энтальпии реакции циклопропана с бромистым водородом, полученные Лейчером, Уолденом, Ли и Парком [834], приводят в величине Д / / / () - 18 6 ккал / молъ. Девис, Лейчер и Парк [308] на основании энтальпии реакции 1-бромпропана с водородом рассчитали значение AHfz93 ( g) - 19 91 ккал / молъ. Рожнов и Андреевский [1259], а также Броуер и Уайтбот [173] измеряли константы равновесия изомеризации до 2-бромпропана. В сочетании со значениями энтропии и энтальпии образования 2-бромпропана, принятыми в данной работе, их результаты приводят к значениям AHfZ9s ( g), равным соответственно - 20 2 и - 20 5 ккал / молъ. Принято среднее взвешенное значение AZT / 98 ( g) - 21 0 ккал / молъ. [13]
Бьеллерап [137] измерял энтальпию сгорания и вычислил A - ff / 9S ( I) - - 29 73 ккал / молъ и & Hf29g ( g) - 21 98 ккал / молъ. Бьеллерап рассчитал также значение &. Лейчером, Кианпуром и Парком [829], а также значение Д / 98 ( g) - 21 15 ккал / молъ по энтальпии реакции между 1-бром-пропаном и водородом на основании неопубликованных данных, сообщенных Лейчером. Более ранние данные по энтальпии реакции циклопропана с бромистым водородом, полученные Лейчером, Уолденом, Ли и Парком [834], приводят в величине AHf29S ( g) - 18 6 ккал / молъ. Девис, Лейчер и Парк [308] на основании энтальпии реакции 1-бромпропана с водородом рассчитали значение Ajff / 298 ( g1) - 19 91 ккал / молъ. Рожнов и Андреевский [1259], а также Броуер и Уайтбот [173] измеряли константы равновесия изомеризации до 2-бромпропана. В сочетании со значениями энтропии и энтальпии образования 2-бромпропана, принятыми в данной работе, их результаты приводят к значениям ДЯ / ав ( g), равным соответственно - 20 2 и - 20 5 ккал / молъ. Принято среднее взвешенное значение АЯ / 298 ( g) - 21 0 ккал / молъ. [14]
Страницы: 1