Константа - равновесие - комплексообразование
Cтраница 1
Константа равновесия комплексообразования зависит от химической структуры углеводородов. Наибольшие значения К имеют м-алканы, причем с увеличением и молекулярной массы константа равновесия увеличивается. Зависимость константы равновесия Образования комплекса от молекулярной массы - алкана линейна. Как видно из рис. 71, извлечение комцлексообразующих углеводородов ( повышение К) с удлинением цепи - алкана происходит быстрее при меньших температурах. Охватывая довольно широкий температурный интервал, эти данные позволяют определять температуру начала образования комплекса карбамида с индивидуальными н-алканам и. Кроме того, они дают возможность определять глубину извлечения - алканов при депарафинизации нефтепродуктов при заданной температуре. [1]
 |
Частота полосы поглощения ОН-группы метанола, ассоциированного с анионами различных солей, в ИК-спектрах СН3ОН в бензоле в зависимости от радиуса аниона. [2] |
Константу равновесия комплексообразования ионных пар с рас творителем можно определить экспериментально, если извести; концентрация сольватированных или свободных ионных пар в си стеме. Пусть X означает свободную ионную пару, Y - ионнук пару, находящуюся в комплексе с п молекулами растворителя S - растворитель. [3]
Расчет константы равновесия комплексообразования радикала I с водой дает значение 1 25 - lQ - 22 см3 / молекула ( 7 5 - Ю 2 л / моль) при 19 С. Энергия водородной связи, найденная из температурной зависимости константы равновесия, составляет 2 4 1 ккал / моль. Следовательно, энергия водородной связи при образовании сольватированных растворителем радикалов примерно равна энергии водородной связи, возникающей между двумя частицами, не имеющими неспаренные электроны. [4]
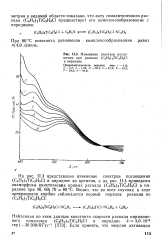 |
Изменение спектров поглощения при распаде ( CsHshT HeCl в пиридине. Продолжительность реакции, мин. / - 1 0. [5] |
При 80 С константа равновесия комплексообразования равна - 4 0 л / моль. [6]
Вычислены приближенные значения констант равновесия комплексообразования. [7]
ИК - и УФ-спектроскопия обладают большими потенциальными возможностями определения констант равновесия комплексообразования ионов в смешанных растворителях. [8]
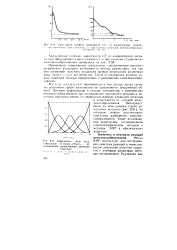 |
Зависимость доли ( ап комплексов Zr Acac M ( Tfac4. от соотношения концентраций лигандов. [9] |
Непосредственно но этим данным строят диаграммы выходов ( рис. 6.51), по которым можно рассчитывать константы равновесия комплексообразования. Такие исследования аналогичны исследованиям спектрографическим методом и методом ЭПР в физическом варианте. [10]
При рассмотрении реакций с образованием КПЗ в качестве промежуточных продуктов следует иметь в виду возможность влияния среды на константу равновесия комплексообразования. При относительно слабых донорах и акцепторах влияние растворителя оказывается не столь существенным [93], однако даже в этом случае вследствие некоторой десольватации донора и акцептора при образовании комплекса ДА должно проявляться изменение константы равновесия при переходе от инертных к сильно сольватирующим растворителям. Ожидать в таких случаях ощутимого влияния диэлектрической проницаемости среды на К не следует. В табл. II.1 приведены данные о влиянии среды на константы комплексообразования некоторых соединений, имеющих неполярную природу. [11]
В последние годы константы равновесия комплексообразования катионов щелочных металлов с различными растворителями в среде ацетонитрила определялись с помощью катиончувстви-тельного стеклянного электрода [43, 53]; было найдено, что значения Ку для катионов лития увеличиваются в ряду пропиленкарбонат-метанол - - вода - пиридин - диметилформамид - формамид - метилформамид - диме-тилсульфоксид-диметилацетамид-гексаметилфосфортриамид. Такое же согласие наблюдается и для других катионов щелочных металлов. Такой же метод использован в работе [54] для исследования ряда аналогичных систем. [12]
Следует, однако, иметь в виду, что химическая реакция сшивания осуществляется в сильно вязкой полимерной среде. Иллюстрацией этого могут служить данные Ворсфолда [3] по влиянию температуры на константу равновесия комплексообразования между полимерными аминной и нитрофенольной группами. При высоких температурах полимерный характер агентов не вносит практически никаких осложнений и мало влияет на величину константы равновесия. Но ситуация резко меняется при переходе через температуру стеклования: сегментальная подвижность резко падает, величина константы также уменьшается по сравнению с тем, что показывают низкомолекулярные агенты, и перестает зависеть от температуры. [13]
Из зависимости обратная величина ускорения - обратная концентрация катализатора ( аналогичная зависимость Лайнуивера - Берка хорошо знакома энзимологам) для катализа 1 5-диметоксинафтали-ном при 85 С можно найти, что максимальная скорость по сравнению с реакцией в отсутствие катализатора в 1900 раз больше и константа связывания равна 1 0 л / моль. Комплексообразование сопровождается изменением поглощения флуоренильного соединения в видимой области, причем установленная спектрофотометрически константа равновесия комплексообразования с фенантреном 3 л / моль хорошо согласуется с величиной 2 8 л / моль, полученной из кинетических данных. Спектральные изменения обычно состоят в появлении или увеличении поглощения в более длинноволновой области, однако в аналогичных комплексах с тринитрофлуореном наблюдается дискретная полоса поглощения переноса заряда. Более того, каталитическая активность, если за меру ее принять логарифм произведения константы образования комплекса на константу скорости его превращения, пропорциональна электронодонорной способности ряда донорных молекул, оцененной из вычисленных энергий наивысшей заполненной молекулярной орбитали или максимума полосы поглощения переноса заряда в комплексах с тетрациано-этиленом и хлоранилом. [14]
Константы р / можно определить с помощью ( 256) или ( 257), как описано выше, графическим или другим методом. Примеров практического применения уравнений ( 256) или ( 257) для определения констант равновесия комплексообразования пока немного, что, по-видимому, объясняется чаще всего необратимостью кинетических волн. При этом во всех случаях были исследованы обратимые кинетические волны, обусловленные замедленной диссоциацией соответствующих компонентов. [15]
Страницы: 1 2