Константа - равновесие - метан
Cтраница 3
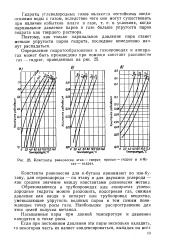 |
Константы равновесия этан - гидрат, пропан - пидрат и н-бу. [31] |
Константы равновесия для н-бутана принимают по изо-бу-тану, для сероводорода - по этану и для двуокиси углерода - как среднее значение между константами равновесия метана. [32]
 |
Влияние давления Р на степень извлечения ( а и удельный расход абсорбента ( б. [33] |
Зависимость между коэффициентом извлечения и давлением ( при постоянных Р, t, n и др.) в интервале 5 - 14 МПа практически линейная - это хорошо согласуется с тем, что с повышением давления уменьшаются константы равновесия метана. [34]
Решение уточняется следующим образом: по составу жидкой фазы с помощью уравнения (11.15) находят среднемассовую критическую температуру условного компонента Q - Далее по уравнению (11.17) или (11.18) уточняют давление схождения, а по уравнению (11.26) или (11.29) - константы равновесия метана и азота. В противном случае итерационные расчеты продолжают, начиная с определения констант равновесия всех компонентов смеси, за исключением метана и азота, для которых эти величины принимают равными их уточненным значениям на предыдущем шаге. [35]
При высоких давлениях константа фазового равновесия метана отклоняется от значений констант равновесия, вычисленных по уравнениям (1.57) и (1.58), а положение ее на графике lg Klt lg p в этой области давлений зависит от давления схождения ( или критического давления), при котором константа равновесия метана становится равной единице. [36]
На рис. IV.2 показана зависимость константы равновесия метана от давления при постоянной температуре ( 60 С) для бинарных смесей метана с различными углеводородами. Значения констант равновесия метана, рассчитанные по составам фаз бинарных смесей, приведены в приложении. [37]
Сравнение различных - методов определения констант равновесия показало, что константы равновесия компонентов от этана до гексана включительно определяются со средней точностью б - 10 % i. Погрешность в определении констант равновесия метана может доходить до 30 % и более. [38]
В абсорберах высокого давления, где константы равновесия метана приближаются к величине, меньшей 10 0, абсорбция метана близ верхней тарелки вызывает значительное повышение температуры. Перепад температур близ нижней тарелки колонны вследствие абсорбции более тяжелых углеводородов также относительно велик. [39]
В результате проведенных исследований была разработана V методика расчета фазовых превращений газоконденсатных систем. Отличительными особенностями этой методики являются: определение константы равновесия метана по составу равновесной жидкой фазы с учетом группового и фракционного состава конденсата, определение давления схождения по составу равновесной жидкой фазы с учетом фракционного состава конденсата, разбивка конденсата на пять фракций и определение констант равновесия этих фракций по их средним ( объемным) температурам кипения. [40]
 |
Влияние давления на степень извлечения ( а, на состав компонентов в поглощенной смеси ( б и на удельный расход абсорбента ( в. [41] |
Зависимость между коэффициентом извлечения и давлением ( при постоянных р, t, n и других параметров) в интервале давлений 5 - 14 МПа практически линейная. Это хорошо согласуется с тем, что с повышением давления уменьшаются константы равновесия метана. [42]
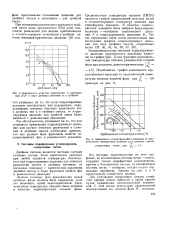 |
Зависимость констант равновесия от давления при 37 8 в двух двойных системах и в тройной.| Зависимость коррелирующего давления от среднемольной температуры кипения. для двойных смесей. [43] |
Двойная система является частным случаем сложных систем. Если критическое давление при любой заданной температуре используется как коррелирующее давление для констант равновесия метана в двойных системах, то последнее совпадает с критическим давлением двойных систем и будет функцией свойств фаз и равновесного давления. [44]
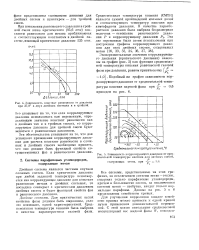 |
Зависимость констант равновесия от давления при 37 8 в двух двойных системах и в тройной.| Зависимость коррелирующего давления от сред-пемолыюй температуры кипения для двойных смесей. [45] |
Страницы: 1 2 3 4