Константа - равновесие - образование
Cтраница 3
К аналогичным выводам приводит и изучение изменения энтропии, а также логарифма константы равновесия образования. [31]
Измеряя уменьшение поглощения карбонильной группы при различных койцентрациях гидроксиламина, можно вычислить константу равновесия образования промежуточного продукта. Вблизи нейтрального значения рН скорость реакции пропорциональна активности ионов водорода, что свидетельствует о кислотном катализе на стадии дегидратации. [33]
Такое же количество азота адсорбировалось из смеси NH3 - Н2 в которой, согласно константе равновесия образования аммиака, парциальное давление азота равнялось давлению в опытах с чистым азотом. [34]
Эти цифры лишь немного меньше представленных в табл. 3.12, которые могут быть обусловлены константой равновесия образования внешнесферного комплекса, меньшей чем единица, для комплексов с нейтральными аминами в качестве лигандов. [35]
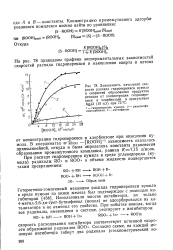 |
Зависимость начальной скорости распада гидроперекиси кумила и скоростей образования продуктов реакции от концентрации гидроперекиси в хлорбензоле в присутствии Ag2O ( 10 г / л при 73 С. [36] |
В координатах ш кЬон - [ ROOH ] 1 зависимость оказалась прямолинейной, откуда и была определена константа равновесия образования промежуточного комплекса, равная / ( 7 15 л / моль. [37]
Важно иметь в виду, что любая измеренная константа равновесия ком-плексообразования в растворе фактически представляет собой сумму констант равновесия образования всех возможных комплексов стехиометрии 1: 1 и только в том случае, когда один из этих комплексов гораздо устойчивее, чем все остальные, наблюдаемая константа равновесия будет равна константе устойчивости соответствующего комплекса. Следовательно, наблюдаемая константа равновесия комплексообразования в растворе может быть больше константы устойчивости комплекса, в котором возникает полоса поглощения переноса заряда, если одновременно образуются и другие комплексы, в которых эта полоса отсутствует. Такая ситуация особенно вероятна в случае, когда энергия образования КПЗ мала, что бывает довольно часто. Если только часть образующихся комплексов обладает поглощением переноса заряда, экспериментально найденный коэффициент экстинкции будет занижен, так как он будет усреднен по всем образующимся комплексам. Фактически при очень слабых взаимодействиях почти все наблюдаемое поглощение переноса заряда может быть обусловлено скорее контактным переносом заряда, чем образованием КПЗ. Это проявляется в непостоянстве экспериментально установленного коэффициента экстинкции комплекса в различных условиях в зависимости от доли поглощающих комплексов. [38]
В некоторых случаях возможно [64] рассчитать значение константы скорости реакции превращения внешнесферного комплекса во внутрисферный, если известна константа равновесия образования ионной пары. Природа вступающей группы играет определенную, хотя и небольшую, роль в определении скорости процесса. Вода обладает статистическим преимуществом в том, что по крайней мере одна молекула воды всегда стоит в правой части уравнения. Анионы могут находиться в положении, удаленном от уходящей молекулы воды. [39]
Авторы провели аналогичные расчеты и по другому уравнению, согласно которому скорость реакции пропорциональна не концентрациям реагентов и константе равновесия образования активированного комплекса [ уравнение (II.4) ], а летучестям реагентов. Оказалось, что такой расчет приводит к ошибочным результатам: константа скорости реакции не возрастала, а уменьшалась с повышением давления. [40]
Но, если значения логарифмов констант равновесия образования углеводородных структурных групп получены на основании достаточно точных данных о логарифмах констант равновесия образования различных углеводородов, то данные о логарифмах констант равновесия образования сульфоновой группы являются менее надежными, так как они получены на основании данных лишь об одном соединении - диметилсульфоне. [41]
Но, если значения логарифмов констант равновесия образования углеводородных структурных групп получены на основании достаточно точных данных о логарифмах констант равновесия образования различных углеводородов, то данные о логарифмах констант равновесия образования сульфоновой группы являются менее надежными, так как они получены на основании данных лишь об одном соединении - диметилсульфоне. [42]
Если хим. р-ция в клетке медленнее, чем диффузия ( к2 / скл), выражение для ( снаб4 упрощается: / сна6л КАВ скл, где КАВ к / 2 по сути, есть константа равновесия образования диффузионной пары. [43]
Константы равновесия образования многих органических веществ из простых веществ для широкого диапазона температур, применительно к состоянию идеального газа, опубликованы в виде таблиц Стал л ом, Уэйлесом и др. Константу равновесия реакции получают, объединяя константы равновесия образования отдельных соединений, входящих в стехиометрическое уравнение. [44]
На самом деле, если вторичный процесс, идущий с участием иона карбония, связанного в ионной паре, медленнее, чем реакции диссоциации и рекомбинации ионной пары, то наблюдаемый порядок брутто-процесса равен двум, а эффективная константа скорости k второго порядка равна kKko, где / С - константа равновесия образования ионных пар, a k o - константа скорости бимолекулярного вторичного процесса. [45]
Страницы: 1 2 3 4