Константа - равновесие - образование - комплекс
Cтраница 2
Для записи уравнения следует ввести коэффициент пропорциональности, который можно включить в константу равновесия образования комплекса. [16]
 |
Зависимость скорости образования тельно, при достаточно боль-радикалов от начальной концентрации fvi. [17] |
Для подтверждения правильности предлагаемой схемы распада гидроперекиси с учетом образования смешанного комплекса измерены константы равновесия образования комплексов Cu. [18]
Трудно сделать исчерпывающее сравнение силы акцепторов, поскольку растворители и температура, которые были использованы при вычислении констант равновесия образования комплексов, изменяются в широких пределах. Более того, значения констант и в некоторых случаях даже порядок, в котором располагаются акцепторы по их силе в данном растворителе, зависят от донора, выбранного в качестве стандарта. В табл. 12 перечислены константы образования ряда комплексов гексаметилбензола с обычно используемыми акцепторами. С той же степенью надежности можно принять, что незначительные температурные изменения мало влияют на приведенные значения Кс - Отсюда следует, что в случае гексаметилбензола в качестве донора и четыреххлористого углерода как растворителя сила акцепторов изменяется в ряду тетрацианэтиленмонохлористый иод 1, 3 5-тринитробензол пикриновая кислотаиодп-бензохинон. В эту серию не включен малеиновый ангидрид, так как значение Кс для его взаимодействия с гексаметилбензолом в четыреххлористом углероде не определено. Однако в случае взаимодействия с пиреном в хлористом метилене [35] и с бензолом в хлороформе [67] этот акцептор приблизительно той же силы, что и / г-бензохинон. [19]
Исследовав зависимость эффективной константы скорости реакции ( в которую входят константы скорости элементарных реакций для всех частиц и константы равновесия образования комплексов с растворителем) от концентрации растворителя в системе, вообще говоря, можно вычислить абсолютные значения констант равновесия и констант скорости элементарных актов. Однако решение такой системы уравнений в общем виде чрезвычайно сложно. Зачастую сольва-тируются растворителем не обе реагирующие частицы ( А и В), а лишь одна из них. [20]
В растворах комплексные соединения находятся в равновесии с образующими их частицами, и наиболее важной характеристикой комплекса является константа равновесия образования комплекса, или константа устойчивости. [21]
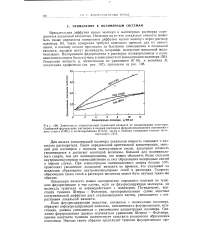
Из зависимости lg / С от температуры для м-алканов ( рис. 70) следует, что с повышением температуры константа равновесия образования комплекса уменьшается и, следовательно, равновесие сдвигается вл. Для каждого углеводорода существует верхний предел температуры, при котором еще может существовать его комплекс с карбамидом. [22]
Ведь до сих пор не существует строгой количественной теории, которая могла бы универсально, с помощью одного уравнения описать зависимость константы скорости реакции и константы равновесия образования комплексов с растворителем от природы среды, в которой протекает реакция. [23]
Если ks k, то k &2 и скорость реакции - это скорость, с которой образуется комплекс. Выражение в скобках представляет собой константу равновесия образования комплекса в отсутствие химических изменений. Обе эти трактовки были первоначально предложены Бьеррумом [10] и Брен-стедом [13] для ионных реакций. [24]
Если к3 к, то к к2 и скорость реакции - это скорость, с которой образуется комплекс. Выражение в скобках представляет собой константу равновесия образования комплекса в отсутствие химических изменений. Обе эти трактовки были первоначально предложены Бьеррумом [10] и Брен-стедом [13] для ионных реакций. [25]
Для статического механизма константа тушения представляет собой константу равновесия образования комплекса в основном состоянии. [26]
 |
Зависимость периода индукции т неинициированного ( а и инициированного АИБН ( б окисления этил-бензола от концентрации л-то луидина при различных начальных концентрациях. [27] |
Подобные зависимости периодов индукции от концентрации амина были получены также для n - анизидина. По-видимому, такое поведение смесей CuSt2 - о-анизидин можно объяснить тем, что константа равновесия образования комплекса о-анизидина с [ CuSt2 ] мала. [28]
Если флуоресцирующие вещества, связанные с молекулами полимера, образуют нефлуоресцирующий комплекс, интенсивность флуоресценции, естественно, должна уменьшаться с увеличением концентрации полимера. Снижение флуоресценции должно подчиняться уравнению Штерна - Фольмера, причем константа тушения соответствует константе равновесия образования комплекса. [30]
Страницы: 1 2 3