Константа - равновесие - реакция - образование
Cтраница 2
Определим зависимость константы равновесия реакции образования дикальцийфосфата от температуры и значение константы равновесия при 122 С. [16]
Полагают, что константа равновесия реакции образования комплекса - К. [17]
Здесь KTk обозначает константу равновесия реакции образования k - ro соединения из r - го соединения в рассматриваемой смеси. [18]
Мы вывели выражение для константы равновесия реакции образования NO в предположении, будто нам известен механизм прямой и обратной реакций на молекулярном уровне. Если бы реакция образования NO осуществлялась в результате простого столкновения двух молекул, такой вывод был бы совершенно правилен. Но подлинный механизм рассматриваемой реакции значительно сложнее. [19]
При температуре 930 К константа равновесия реакции образования водяного газа ( CO H2O: z C02 - - №) равна единице. Смесь, состоящая из 20 % окиси углерода и 80 % водяного пара, нагревается до 930 К. Требуется определить состав смеси при равновесии. [20]
При температуре 930 К константа равновесия реакции образования водяного газа ( СО Н2О СО2 Н2) равна единице. Смесь, состоящая из 20 % окиси углерода и 80 % водяного пара, надевается до 930 К. Требуется определить состав смеси при равновесии. [21]
В, по которым рассчитываем константы равновесия реакций образования 2, 4, 4-триметилпентенов. [22]
Кг, и в - константы равновесий реакций образования соответствующих изомеров сульфокислоты из нафталина. В явном противоречии с этими данными находятся попытки этого исследователя 91 установить величину константы равновесия сульфирования нафталина. Опыты, проводившиеся при других температурах, указывают на уменьшение константы равновесия с уменьшением концентрации серной кислоты. [23]
В табл. 49 приведены значения констант равновесия реакции образования С2Н2 из элементов и-феакшш СН4м 2Н2 ЗН2, а в габл. [24]
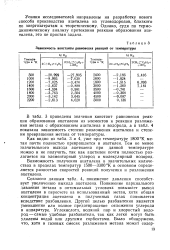 |
Зависимость константы равновесия реакций от температуры. [25] |
В табл. 3 приведены значения констант равновесия реакции образования ацетилена из элементов и реакции разложения метана с образованием ацетилена и водорода, а в табл. 4 показана зависимость степени разложения ацетилена и степени превращения метана от температуры. [26]
На основании полученных данных были вычислены константы равновесия реакции образования комплекса с ацетатом ртути для замещенных циклопропанов, а также определена зависимость этих констант от температуры, что позволило подсчитать теплоту образования комплексов. [27]
Полученные экспериментальные данные позволяют также определить константу равновесия реакции образования комплекса и число молекул органической кислоты, принимающих участие в этой реакции. [28]
Константа равновесия реакции может быть выражена через константы равновесия реакций образования веществ, участвующих в реакции. Действительно, из выражений ( 480) и ( 482) видно, что In / Ср представляет собой изменение функции состояния и поэтому определяется только начальным и конечным состояниями системы и не зависит от промежуточных состояний, через которые проходит система. [29]
Постоянные consti и const2 уравнения (5.37) зависят от констант равновесия реакций образования ионных тройников и от предельных значений молярных электропроводиостей частиц КА, К2А и К. Согласно уравнению (5.37) кривая электропроводность - концентрация проходит через минимум. [30]
Страницы: 1 2 3 4