Константа - равновесие - реакция - гидрирование
Cтраница 1
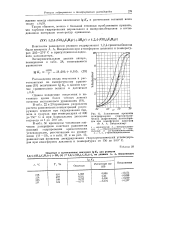 |
Равновесные проценты дегидрирования гидроароматических ( нафтеновых углеводородов при атмосферном давлении по А. А. Введенскому. [1] |
Константы равновесия реакции гидрирования 1 2 4-триметилбензола были измерены А. А. Введенским при атмосферном давлении и температурах 205 - 274 С в присутствии палладие-вого катализатора. [2]
Константы равновесия реакций гидрирования ( рис. 18) достаточно высокие. И равновесие практически полностью сдвинуто в сторону образования сероводорода / IOJ, но степень гидрогенолиза определяется кинетикой процесса. [3]
Пиз и Дарген [23] измерили константы равновесия реакции гидрирования этилена в интервале температур от 600 до 700 С при атмосферном давлении в отсутствии катализатора. [5]
В табл. 30 приведены численные значения логарифмов констант равновесия реакций гидрирования ароматических углеводородов, рассчитанные по уравнениям ( 11 - 19), а в табл. 31 и на рис. 13, равновесные проценты дегидрирования гидроароматических углеводородов при атмосферном давлении и температурах от 150 до 500 С. [6]
Там же приведена более полная сводка Экспериментальных данных по измерению констант равновесия реакции гидрирования этилена. [7]
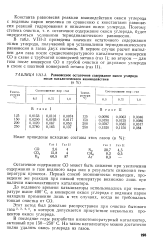 |
Равновесное остаточное содержание окиси углерода после каталитического взаимодействия. [8] |
Константа равновесия реакции взаимодействия окиси углерода с водяным паром невелика по сравнению с константами равновесия реакций гидрирования и окисления окиси углерода. [9]
На основании величин Ф - потенциалов и теплот образования из элементов, приведенных для н-алкилбензолов и н-алкилциклогексанов на стр. Справочника, нами вычислены константы равновесия реакций гидрирования бензола, толуола, этилбензола и н-пропилбензола, протекающих в паровой фазе. Эти данные приводятся в табл. 85, где они сравниваются с величинами, вычисленными по приведенным выше эмпирическим уравнениям. [10]
В процессе гидрирования ароматических углеводородов при высокой температуре довольно интенсивно протекает реакция дегидрирования, и по мере приближения к равновесию суммарная скорость превращения ароматических углеводородов в нафтеновые уменьшается. При высоких температурах, когда константа равновесия реакции гидрирования мала, скорость обратной реакции с увеличением степени превращения быстро возрастает. В результате ускорение прямой реакции, происходящее при повышении температуры, нейтрализуется. [11]
Из этих данных видно, что при температурах, представляющих практический интерес, равновесие реакций гидрирования сернистых соединений смещено в сторону углеводородов и сероводорода; для меркаптанов, сульфидов и дисульфидов с повышением температуры убыль энергии Гиббса при гидрировании увеличивается. Особенно сильно снижается с увеличением температуры константа равновесия реакции гидрирования метилтиофена. Для других тиофенов термодинамические данные отсутствуют. Оценочные расчеты показывают, что для них константы равновесия гидрирования с увеличением температуры также сильно снижаются. Для всех сераорганических соединений, кроме тиофенов, термодинамические ограничения гидрирования в интервале 300 - 800 К отсутствуют. [12]
При процессах гидрирования следует ожидать увеличения скорости реакции с повышением температуры. В случае гидрирования ароматических углеводородов при высокой температуре сравнительно интенсивно протекает обратная реакция, и по мере приближения к равновесию суммарная скорость превращения уменьшается. При высоких температурах, когда константа равновесия реакции гидрирования мала, скорость обратной реакции быстро возрастает с увеличением степени превращения. Это явление нейтрализует ускорение прямой реакции под действием температуры. Результаты гидрирования в лабораторном масштабе каталитического газойля промежуточного основания ( 293 - 404 С) в присутствии различных катализаторов под избыточным давлением 52 5 am показали, что при температурах выше 370 С восстановление бициклических ароматических углеводородов лимитируется устанавливающимся равновесием. Аналогичные результаты были получены [19] и при исследовании гидрирования нафталина, фенантрена и пирена. В области температур до 370 С восстановление бициклических ароматических углеводородов увеличивается с повышением температуры вследствие влияния ее на скорость. Поскольку степень обессеривания не лимитируется равновесием, при высоких температурах достигается более полное удаление серы. [13]
На основании величины AHv Mg 8 34 ккал / молъ, установленной Никерсоном и др. [1068], получено значение AHfl ( g) - 56 97 ккал / молъ. Зинке и Оттинг [1358] приводят ссылки на предшествующие работы по изучению этого соединения. Бакли и Херингтон [180] определили константы равновесия реакции гидрирования бутанона-2 до бутанола-2. Результаты этих исследователей прекрасно согласуются с принятыми нами значениями. Ссылки на более ранние работы по изучению равновесной реакции гидрирования приведены в работе Бакли и Херингтона. Согласно Никерсону и др. [1068], ТЪ 352 61 К, при этом АТ / г; 7 475 ккал / молъ. По данным измерений Кобе, Кроуфорда и Стефен-сона [773], Тс 535 7 К и Рс 41 атм. [14]
На основании величины & Hv 2gs 8 34 ккал / молъ, установленной Никерсоном и др. [1068], получено значение & HfM9 ( g) - 56 97 ккал / молъ. Зинке и Оттинг [1358] приводят ссылки на предшествующие работы по изучению этого соединения. Бакли и Херингтон [180] определили константы равновесия реакции гидрирования бутанона-2 до бутанола-2. Результаты этих исследователей прекрасно согласуются с принятыми нами значениями. Ссылки на более ранние работы по изучению равновесной реакции гидрирования приведены в работе Бакли и Херингтона. Согласно Никерсону и др. [1068], ТЪ 352 61 К, при этом kHv 7 475 ккал / молъ. По данным измерений Кобе, Кроуфорда и Стефен-сона [773], Тс 535 7 К и Рс 41 атпм. [15]
Страницы: 1
