Константа - равновесие - обменная реакция
Cтраница 1
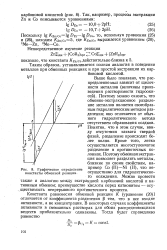 |
Графическое определение константы обменной реакции. [1] |
Константа равновесия обменной реакции К ( уравнение ( 20) ] отличается от коэффициента разделения ( 3 тем, что в нее входят активности, а не концентрации. В некоторых случаях коэффициенты активности в смешанных растворах для обоих распределяющихся веществ приблизительно одинаковы. [2]
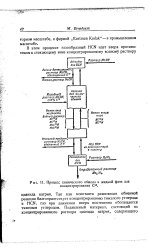 |
Процесс химического обмена в жидкой фазе для концентрирования С13. [3] |
Так как константа равновесия обменной реакции благоприятствует концентрированию тяжелого углерода в HCN, газ при движении вверх постепенно обогащается тяжелым углеродом. [4]
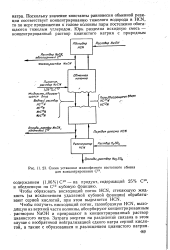 |
Схема установки жидкофазного изотопного обмена для концентрирования С13. [5] |
Поскольку значение константы равновесия обменной реакции соответствует концентрированию тяжелого водорода в HCN, то по мере продвижения к голове колонны пары постепенно обогащаются тяжелым углеродом. [6]
Коэффициент разделения однозначно связан с константой равновесия обменной реакции. Эта связь будет ниже подробно рассмотрена. Ограничимся здесь указанием на то, что величина х близка к единице, однако точно не равна ей. [7]
Представляло интерес использовать метод газо-жидкостной хроматографии для определения констант равновесия обменных реакций при синтезе ангидридов из уксусного ангидрида и пропионо-вой или масляной кислоты. [8]
Многих исследователей привлекает также возможность использования составов сосуществующих минералов в качестве геологических термометров для определения температур их образования, основанная на представлении о том, что коэффициенты разделения и константы равновесия гипотетических обменных реакций между сосуществующими минералами переменного состава являются функциями только температуры. Однако, как видно из полученных изотерм распределения катионов между сосуществующими цеолитами ( см. рис. 34), и коэффициенты разделения, и константы обменного равновесия изменяются с изменением содержания обменивающихся компонентов в твердой фазе. Кроме того, распределение катионов между цеолитами практически не зависит от температуры. Поэтому сосуществующие высококремнистые цеолиты не могут служить для оценки физико-химических условий цеолитообразования. [9]
Следовательно, не только перемешивание, но и температура при обменной экстракции, связанной с химической реакцией, является фактором, повышающим эффективность промышленных аппаратов. При этом следует отметить, что константа равновесия обменных реакций, как правило, уменьшается с повышением температуры. В данном случае необходимо определять оптимальную температуру. [10]
При изотопном уравновешивании отношения концентраций водорода и дейтерия в газообразной фазе над металлом и растворенных в металле, вообще говоря, не одинаковы. Распределение изотопов между двумя фазами зависит как от их молекулярных и атомных констант, так и от экспериментальных условий - в первую очередь от температуры. Зная константу равновесия обменной реакции, всегда можно по известным концентрациям изотопов в газовой фазе вычислить отношение полного числа атомов водорода к полному числу атомов дейтерия и, зная далее полное число атомов дейтерия, первоначально введенное в обменник, можно определить интересующее нас полное число атомов водорода, первоначально находившееся в навеске металла. Однако теоретический расчет константы равновесия или ее экспериментальное определение представляют сложную задачу. [11]
Данный ряд может пополняться и другими металлами, которые сообразно своим свойствам займут соответствующее место. Металл, обладающий большей экстрагируемостью, вытесняет из органической фазы металл, имеющий меньшую экстрагируемость. В качестве мерила экстрагируемое можно принять константу равновесия обменных реакций с водородом или с каким-нибудь одним металлом ряда. [12]
 |
Коэффициенты электролитического разделения изотопов. [13] |
Однако обращение с большими количествами жидкого водорода создает значительные осложнения. Этот способ, без промежуточного высокотемпературного катализа, может дать не выше 50 % D в виде чистого HD, так как при очень низкой температуре обменная реакция На Da 2HD не идет. Были также разработаны методы, основанные на сильной зависимости константы равновесия обменной реакции НаО ( жидк. [14]
Страницы: 1