Константа - равновесие - обратимая реакция
Cтраница 1
Константа равновесия обратимой реакции ( в нашем случае диссоциации) показывает, насколько реакция смещена в ту или другую сторону при данной температуре. Константа, характеризующая прямую реакцию, есть отношение произведения давлений ( концентраций) конечных продуктов к исходным с учетом соответствующих коэффициентов. [1]
В отличие от констант равновесия других обратимых реакций, величина К называется в данном случае константой, диссоциаций электролита. Она характеризует склонность его к ионизации. Чем больше ее величина, тем сильнее диссоциирует слабый электролит и тем выше концентрации ионов его в растворе при равновесии. [2]
Нашей задачей является предсказание констант равновесия Ке обратимых реакций и констант скоростей kr необратимых реакций. [3]
Чему равна при 25 С константа равновесия обратимой реакции, для которой значение AG e равно: а) 5 714 кДж / моль, б) - 5 714 кДж / моль. [4]
Таким образом, при постоянной температуре константа равновесия обратимой реакции представляет собой постоянную величину, показывающую то соотношение между концентрациями продуктов реакции ( числитель) и исходных веществ ( знаменатель), которое устанавливается при равновесии. [5]
Таким образом, при постоянной температуре константа равновесия обратимой реакции представляет собой постоянную величину, показывающую то соотношение между концентрациями про дуктов реакции ( числитель) и исходных веществ ( знаменатель), которое устанавливается при равновесии. [6]
Таким образом, при постоянной температуре константа равновесия обратимой реакции представляет собой постоянную величину, показывающую то соотношение между концентрациями продуктов реакции ( числитель) и исходных веществ ( знаменатель), которое устанавливается при равновесии. [7]
Таким образом, при постоянной температуре константа равновесия обратимой реакции представляет собой постоянную величину, показывающую то соотношение между концентрациями продуктов реакции ( числитель) и исходных веществ ( знаменатель), которое устанавливается при равновесии. [8]
Величина / СДИс, в отличие от констант равновесия других обратимых реакций, называется константой диссоциации электролита. [9]
 |
Схема аппарата с магнитным приводом для выращивания монокристаллов по методу Чохраль-ского. [10] |
Таким образом, возможность транспортных реакций основывается на зависимости константы равновесия обратимой реакции от температуры. Направление переноса вещества определяется знаком теплового эффекта реакции. В экзотермических реакциях оно переносится от более низкой температуры к более высокой, в эндотермических - наоборот. [11]
Этим соотношением можно пользоваться для расчета изобарного потенциала, если известна константа равновесия обратимой реакции. [12]
Вычислите константы образования fet и разложения fe2 этилформиа-та в этом растворе и константу равновесия обратимой реакции К, если концентрации воды, этанола и ионов водорода постоянны. [13]
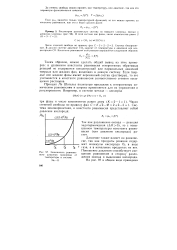 |
Зависимость равновесного давления кислорода от температуры в системе Me-О. [14] |
Таким образом, можно сделать общий вывод из этих примеров: в уравнении константы равновесия гетерогенных обратимых реакций не содержится концентраций или парциальных давлений твердых или жидких фаз, входящих в данную систему. Если твердые или жидкие фазы имеют переменный состав ( растворы), то это учитывается в константе равновесия соответственно степени насыщения растворов. [15]
Страницы: 1 2