Константа - равновесие - система
Cтраница 2
Жидкостная адсорбционная хроматография ( ЖАХ) основана на различии в константах равновесия системы компонент в растворе - адсорбент для разделяемых компонентов раствора. Теория селективности ЖАХ должна основываться на теории адсорбции из бинарных и более сложных жидких растворов. Из-за отсутствия количественной теории разбавленных растворов, а тем более адсорбции из растворов, коэффициенты активности компонентов раствора в адсорбированном состоянии и константы равновесия определяют из экспериментальных изотерм адсорбции. Энергия адсорбции веществ из растворов определяется разностью энергий межмолекулярного взаимодействия его молекул с адсорбентом и с соседними молекулами со стороны объема раствора, поэтому она может быть в несколько раз меньше энергии адсорбции того же компонента из газовой фазы. Жидкостная хроматография может быть использована для изучения адсорбции из растворов и определения константы Генри и изотермы адсорбции из растворов тремя путями. Во-первых, константа Генри и изотерма адсорбции из растворов, особенно в области весьма малых концентраций, могут быть определены из самих хроматограмм адсорбата ( положительно адсорбирующееся вещество из разбавленных растворов) при элюи-ровании из колонны, заполненной исследуемым адсорбентом, растворителем. В-третьих, жидкостная хроматография на аналитических колоннах ( с тем же или другим адсорбентом) может быть использована в качестве вспомогательного аналитического метода для определения концентраций равновесных растворов над изучаемым адсорбентом при статических определениях изотермы адсорбции, когда равновесие заведомо достигается. [16]
Таким образом, если известны суммы состояний, то можно определить константу равновесия системы, а также изменение свободной энергии реакции и другие термодинамические величины. [17]
Жидкостно-адсорбционная молекулярная хроматография в ее приближающемся к равновесному варианте основана на различии в константах равновесия системы раствор - адсорбент для разных компонентов раствора. Даже при полном разделении компонентов смеси при прохождении данного компонента через слой адсорбента в колонне раствор содержит по крайней мере два вещества: компонент анализируемой смеси и растворитель. Таким образом, теория равновесной жидкостно-адсорбционной хроматографии должна основываться на теории адсорбции из бинарных [1 -16] и более сложных [1, 4, 17, 18] жидких растворов. Эта теория разработана еще недостаточно и носит чисто термодинамический характер. Поэтому коэффициенты активности компонентов раствора в адсорбированном состоянии и константы равновесия определяются из самих экспериментальных изотерм адсорбции. Константы равновесия при упрощенных представлениях о структуре адсорбционного слоя могут быть определены через разности работ смачивания чистыми жидкими компонентами, которые, в свою очередь, могут быть найдены из разности работ насыщения адсорбента парами чистых жидких компонентов и их поверхностных натяжений. Однако все это ограничивает возможности расчета и делает его неточным. [18]
Жидкостно-адсорбционная молекулярная хроматография в ее варианте, приближающемся к равновесному, основана на различии в константах равновесия системы раствор - адсорбент. Даже при полном разделении компонентов смеси при прохождении пика данного компонента раствор содержит по крайней мере два вещества: компонент анализируемой смеси и растворитель-элюент. [19]
Если бы происходило только переалкилирование, то различные смеси должны были бы стремиться к составу, определяемому константой равновесия системы. Для данной системы, рассматриваемой при постоянной температуре, константа равновесия имеет определенное значение и фигуративные точки различных равновесных смесей должны лежать на одной кривой. Несмотря на деалкили-рование, экспериментальные данные позволяют разграничить область, в которой находится кривая, соответствующая равновесию переалкилирования. [20]
Карсон и Катц полагают, что гидраты, возникающие из природного газа, насыщенного водой, есть твердые растворы и имеют определенные константы равновесия системы пар-твердое вещество. [21]
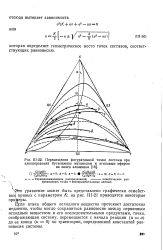 |
Перемещения фигуративной точки системы при. [22] |
Если атака общего исходного вещества протекает достаточно медленно, чтобы могло сохраниться равновесие между первичным исходным веществом и его последовательными продуктами, точка, отображающая систему, перемещается с начала реакции ( и а) до ее конца ( и 0) по траектории, определенной константой равновесия системы. [23]
Во всех уравнениях химической кинетики фигурируют концентрации реагирующих веществ. В термодинамике же константа равновесия неидеальной системы выражается через активности. Это обстоятельство необходимо учитывать, если в кинетическое уравнение входит константа равновесия. Правда, при реакциях в газовой фазе и между нейтральными молекулами в растворе в этом нет практической необходимости, но при рассмотрении реакций между заряженными частицами подобное пренебрежение может явиться источником существенных ошибок. [24]
Во всех уравнениях химической кинетики фигурируют концентрации реагирующих веществ. В термодинамике же константа равновесия иеидеальной системы выражается через активности. Это обстоятельство необходимо учитывать, если в кинетическое уравнение входит константа равновесия. Правда, при реакциях в газовой фазе и между нейтральными молекулами в растворе в этом нет практической необходимости, но при рассмотрении реакций между заряженными частицами подобное пренебрежение может явиться источником существенных ошибок. [25]
Аналогично можно дать количественную трактовку принципа Ле Шателье при изменении концентраций веществ ( или давления) в системе. Для этого необходимо выписать выражение для константы равновесия системы и, помня, что она не зависит от концентраций веществ, подставить в это выражение измененные концентрации. Тогда из условия постоянства константы равновесия, входящие в выражение для константы концентрации веществ примут такие значения, чтобы их отношение осталось тем же самым. [26]
Не имеет большого значения, какую концентрацию аммиака, [ NH3 ] или [ МН3 ], использовали для вычисления значений а. Следовательно, практически можно пользоваться кажущейся концентрацией аммиака в уравнении константы равновесия системы розео-ион - аммиак, особенно в случае, когда общая концентрация аммонийной соли относительно мала. [27]
Не имеет большого значения, какую концентрацию аммиака, [ NHs ] или [ NH3 ], использовали для вычисления значений а. Следовательно, практически можно пользоваться кажущейся концентрацией аммиака в уравнении константы равновесия системы розео-ион - аммиак, особенно в случае, когда общая концентрация аммонийной соли относительно мала. [28]
Состав и количество растворенного газа изменяются, если при данных давлении, температуре и содержании соли в равновесии с водой находится природный газ. В этих условиях насыщенность воды в состоянии равновесия и состав растворенного газа характеризуются константами равновесия системы пар - жидкость. В Венгрии на основании данных исследований подобных систем были сделаны следующие выводы. [29]
Наиболее надежные результаты могут быть получены при использовании уравнений Редлиха - Квонга, Бенедикта - Вебба - Рубина или других точных уравнений состояния [ уравнение ( VI. Выражения на основе уравнения Редлиха - Квонга просты и достаточно иадежны при определении fi для расчета констант равновесия системы жидкость - пар. Уравнение Бенедикта - Вебба - Рубина более сложно в использовании. Метод Редлиха - Квонга применим к неполярным Или слабополярным соединениям и его. [30]
Страницы: 1 2 3