Константа - равновесие - адсорбция
Cтраница 1
Константы равновесия адсорбции К ( и KI вычисляются из равенства химических потенциалов молекул в газовой фазе и в адсорбированном состоянии. [1]
Приведены константы равновесия адсорбции на крекирующих центрах для некоторых чистых углеводородов и соединений кислорода, серы и азота. Некоторы - е расчеты сделаны на основании литературных данных. Для нескольких изученных соединений были определены константы равновесия при различных температурах. Рассчитаны теплоты и энтропии адсорбции на крекирующих центрах поверхности. [2]
Определены константы равновесия адсорбции, скорости реакции и энергии активации изученных реакций. Найдено, что реакции изомеризации протекают по первому порядку относительно реагирующих олефинов. В свете полученных; результатов обсуждается механизм изученных реакций. [3]
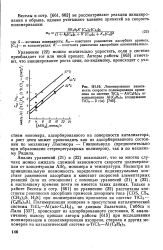 |
Лэнгмюровская зависимость скорости полимеризации пропилена на системе TiCl3 - Al Hsb от концентрации А1 ( С2Н5 з ( содержание TiCl3 - 2 г / л. [4] |
Кя - константа равновесия адсорбции примеси, [ Сп ] - ее концентрация; К - константа равновесия адсоробции алкшинийалкила. [5]
К представляет собой избирательную константу равновесия адсорбции органического компонента из бинарного водного раствора. [6]
 |
Изотерма полимолекулярной адсорбции. [7] |
Постоянная С равна отношению констант равновесия адсорбции ( с мономолекулярным слоем) и конденсации пара. [8]
Постоянная С равна отношению констант равновесия адсорбции ( мономолекулярной) и конденсация пара. [9]
На основе изложенного метода расчета констант равновесия адсорбции оценен состав адсорбционных слоев на гранях ( 111) As и ( 111) Ga ( In) кристаллов GaAs и InAs в газотранспортных системах Ga - As - Cl - Н и In - As - Cl - H. Предполагалось, что As3 и As4 могут сорбироваться сразу на трех центрах, которые образуют треугольник из соседних центров адсорбции. Такой вариант адсорбции исключает из числа возможных площадок адсорбции 13 соседних треугольников. Предполагалось также, что из всех молекулярных форм мышьяка на поверхности ( 111) As могут сорбироваться только молекулы As3, имеющие свободные связи. В расчетах использовались энергии десорбции молекул As3 и As4 с трех центров, равные 293 Дне / моль. [10]
Постоянная К имеет физический мысл константы равновесия адсорбции. [11]
Рт диена и моноена соответственно, a bd и Ьт представляют собой константы равновесия адсорбции. Сходство между уравнениями ( 11) - ( 12) и ( 13) - ( 14) обусловлено тем, что активные центры гетерогенного катализатора всегда присутствуют в количествах, пренебрежимо малых по сравнению с количеством субстрата. [12]
Рт диена и моноена соответственно, a & j и Ьт представляют собой константы равновесия адсорбции. Сходство между уравнениями ( 11) - ( 12) и ( 13) - ( 14) обусловлено тем, что активные центры гетерогенного катализатора всегда присутствуют в количествах, пренебрежимо малых по сравнению с количеством субстрата. [13]
Учитывая эти данные, Морроу и др. [23] исследовали влияние ионной силы раствора на константу равновесия адсорбции и на константу скорости десорбции р-галактозидазы на сефарозе с присоединенным к ней бис - ( 3-аминопропил) амином. Около 90 % фермента, пропущенного через колонку, не задерживаются и только 10 % остаются связанными в колонке посредством электростатических связей и могут быть элюированы растворами с высокой ионной силой, например 1 М хлористым натрием. На основании этих результатов можно сделать вывод, что в данных условиях аминная часть ли-ганда мало участвует в связывании фермента. При хроматографии 3-галактозидазы в аналогичных условиях ( единственное отличие состояло в том, что к 0 05 М трис - НС1 - буферу не добавлялись соли) почти весь нанесенный фермент был неспецифически связан в колонке; 85 % фермента десорбировалось при увеличении ионной силы буферного раствора добавлением 1 М хлористого натрия. Очень хорошие результаты получались, если связывание ( 3-галактозидазы на замещенном геле проводилось при высокой ионной силе ( 1 8 М фосфатный буферный раствор), а последующее элюи-рование при помощи растворов с понижающимся линейным градиентом ионной силы. [14]
Если выражения в скобках представляют активности, то величины К являются константами химического равновесия; если же эти выражения соответствуют концентрациям, то величины К - константы равновесия адсорбции, которые изменяются с концентрацией и составом проходящего раствора. [15]
Страницы: 1 2