Константа - адсорбционное равновесие
Cтраница 1
Константа адсорбционного равновесия для изотермы адсорбции условного компонента может быть найдена по методу, описанному в гл. [1]
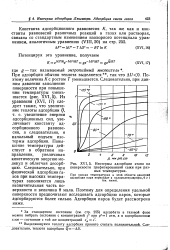 |
Изотермы адсорбции этана на поверхности графитированной сажи при разных температурах. [2] |
Константа адсорбционного равновесия Л, так же как и константы равновесий различных реакций в газах или растворах, связана со стандартным изменением изохорного потенциала уравнением, аналогичным уравнению ( VIII, 20) на стр. [3]
Константа адсорбционного равновесия, связанная со стандартным уменьшением свободной мольной энергии адсорбции - & F выражением (IV.41), может быть представлена в виде отношения активностей компонента в адсорбционной фазе aj и в равновесном объемном растворе а. Активности компонента в каждой фазе могут быть выражены через его концентрации и соответствующие коэффициенты активности. [4]
Константа адсорбционного равновесия для изотермы адсорбции условного компонента может быть найдена по методу, описанному в гл. [5]
Константа адсорбционного равновесия Д и величина адсорбции А зависят от когезионного взаимодействия между молекулами адсорбата. К) и соответственно уменьшается величина А при мономолекулярной адсорбции. При полимолекулярной адсорбции величина адсорбции А может увеличиться с усилением когезионного взаимодействия ад-сорбат-адсорбат. При значительных когезионных взаимодействиях конденсация адсорбированного вещества на поверхности наступает при меньших давлениях, чем для веществ, проявляющих малые когезионные силы. В связи с этим возможны случаи, когда константа адсорбционного равновесия для одного вещества больше, чем для другого, а величина полимолекуляр-пой адсорбции А, начиная с некоторых давлений, для первого вещества меньше, чем для второго. [6]
Константа адсорбционного равновесия и аттракционная постоянная влияют на характер концентрационной кривой, построенной по измерению адсорбционных пиков в осциллографической полярографии. Поэтому в ос-циллополярографических исследованиях необходимо знать величины В и у. Изотерма Фрумкина имеет S-образную форму. [7]
Константа адсорбционного равновесия Ki может быть определена в результате интегрирования кинетического уравнения ( по степени превращения реагирующих веществ в слое катализатора), составленного в соответствии с полной кинетической схемой, в которой учтена обратная реакция. [8]
Величина константы адсорбционного равновесия может быть определена из уравнения избирательной изотермы адсорбции растворенного вещества либо из уравнения парциальной изотермы адсорбции компонента раствора. [9]
Рассчитайте константу адсорбционного равновесия и предельную величину адсорбции, если процесс сорбции описывается уравнением Ленгмюра. [10]
В - константа адсорбционного равновесия; С - концентрация ингибитора; 6 - степень заполнения поверхности молекулами ингибитора; а - аттракционная постоянная; f - фактор энергетической неоднородности; Smax и Smin - константы адсорбционного равновесия, соответствующие максимальным и минимальным значениям энергии адсорбции. [11]
К - константа адсорбционного равновесия; F0 - объемная скорость газа-носителя, приведенная к нормальным условиям; а - степень превращения; т - масса катализатора. [12]
Как зависит константа адсорбционного равновесия b от температуры при адсорбции газа на твердом адсорбенте. [13]
В - константа адсорбционного равновесия, связанная с химической компонентой энергии адсорбции. [14]
В - константа адсорбционного равновесия, связанная с химической частью энергии адсорбции. [15]
Страницы: 1 2 3 4