Константа - скорость - сорбция
Cтраница 1
Константа скорости сорбции, характеризующая химическую активность вещества, определяется экспериментально. [1]
 |
Кажущаяся энергия активации ( кал / моль. [2] |
Константы скорости сорбции La3, Nd31, Gd3 на одной и той же смоле при прочих постоянных условиях практически одинаковы. Скудные данные, имеющиеся в литературе, позволяют предполагать, что в таком же порядке изменяются радиусы связанных со смолой одновалентных катионов. Падение константы скорости сорбции в порядке уменьшения радиуса иона-партнера хорошо согласуется с диффузионным механизмом процесса. [3]
В таблице приведены константы скорости сорбции от дисперсности ионита и температуры. [4]
Расчитанные порядок реакции и константа скорости сорбции выделены курсивом. [5]
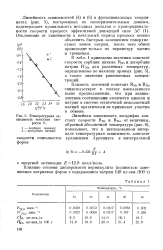 |
Температурная зависимость констант скорости R.| Температура, С. [6] |
В табл. 1 приведены значения констант скорости сорбции никеля RNJ и десорбции натрия R NB Для различных температур, определенные по наклону прямых ( рис. 5), а также значения равновесных концентраций. [7]
Здесь Г - параметр Генри; YI - константа скорости сорбции; се - концентрация в жидкой фазе, равновесная 6е; cs - предельная концентрация при t - сю. [8]
Временным параметром, имеющим строгий физический смысл, является среднее время сорбции, которое из (7.21) по общему правилу определения ( среднего) равно tpl / a, где а - константа скорости сорбции. [9]
Так как скорость адсорбции и ионного обмена контролируется диффузией, то влияние температуры на константы скоростей этих процессов определяется зависимостью коэффициентов BHeuiiici f и внутренней диффузии от температуры и функциональной связью 0 Ш4 Т / Т между константами скоростей сорбции и коэффициентами диффузии. [10]
Константы скорости сорбции La3, Nd31, Gd3 на одной и той же смоле при прочих постоянных условиях практически одинаковы. Скудные данные, имеющиеся в литературе, позволяют предполагать, что в таком же порядке изменяются радиусы связанных со смолой одновалентных катионов. Падение константы скорости сорбции в порядке уменьшения радиуса иона-партнера хорошо согласуется с диффузионным механизмом процесса. [11]
Рассмотрение различных ступеней переноса вещества ( компонентов питательной среды) к метаболизирующей особи популяции ( газообразная фаза - жидкая фаза; жидкая фаза - твердая фаза) показывает, что во многих случаях лимитирующим может быть процесс сорбции или десорбции газообразных веществ. Вот почему успех переноса микробиологического синтеза в аппараты больших размеров во многом обусловлен именно тем, в какой степени интенсивность газового массообме-на обеспечит как питательные потребности особей растущей популяции, так и удаление газообразных продуктов метаболизма этой популяции, необходимое в ряде случаев для поддержания постоянства условий культивирования. Уровень необходимой интенсивности массообменных процессов может быть определен из величин констант скоростей сорбции, полученных из основной модели микробиологического синтеза. [12]
Этот метод разработан группой сотрудников института горного дела им. Метод предназначен для характеристики химической активности каменных углей, углистых пород, сульфидов и других природных материалов. По химической активности определяют относительную склонность таких материалов к самовозгоранию. Скорость окисления зависит от концентрации кислорода, которая в объеме материала является непостоянной, поэтому авторы предложили определять константу скорости окисления численно равной константе скорости сорбции кислорода, которая не зависит от концентрации кислорода, но зависит от температуры, дисперсности и других свойств материала. Чтобы получить сравнимые результаты, которые можно использовать на практике, условия определения константы скорости окисления U [ мл / ( г-ч) ] в опыте должны был близки действительным. Полученные результаты служат для оценки относительной склонности материалов к самовозгоранию, расчета скоростей окислительных процессов и определения стойкости материалов при хранении. Сущность метода заключается в следующем. [13]
Страницы: 1