Константа - скорость - отдельная стадия
Cтраница 1
Константы скоростей отдельных стадий ku k2 и k3 могут иметь очень различные значения. Рассмотрим два предельных случая, которые встречаются особенно часто. В зависимости от отношения скоростей образования и разложения различают, по Скрабалю, промежуточные вещества Аррениуса и промежуточные вещества Вант-Гоффа. [1]
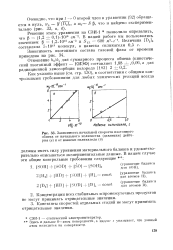 |
Зависимость начальной скорости изотопного обмена от начального количества ( давления дейтерия ( а и от навески силикагеля ( б. [2] |
Константы скоростей отдельных стадий не могут принимать отрицательные значения. [3]
Константы скорости отдельных стадий реакции могут быть вычислены, если известна концентрация фермента, на основании соотношений, приведенных на стр. [4]
Найдены константы скоростей отдельных стадий процесса эпоксидирования, константы диссоциации комплексе гидроперекись трет-бутила - катализатор и трет-бутиловын спирт - катализатор. [5]
Найдены константы скоростей отдельных стадий процесса эпоксидирования, константы диссоциации комплеков гидроперекись трет-бутила - катализатор и трет-бутиловый спирт - катализатор. [6]
Известна схема реакции и величины констант скорости отдельных стадий. Требуется рассчитать концентрацию того или иного компонента в некоторый момент времени или установить время, за которое концентрация того или иного компонента достигает определенного значения. Для этого достаточно найти уравнение кинетической кривой по интересующему исследователя продукту. [7]
Известна схема реакции и величины констант скорости отдельных стадий. Требуется рассчитать концентрацию того или иного компонента в определенный момент времени или определить время, за которое концентрация того или иного компонента достигнет определенного значения. Для этого достаточно найти уравнение кинетической кривой интересующего нас продукта, причем с успехом можно применять численное интегрирование. [8]
Известна схема реакции и величины констант скоростей отдельных стадий. Требуется рассчитать концентрацию того или иного компонента в определенный момент времени или определить время, за которое концентрация того или иного компонента достигнет определенного значения. Для этого достаточно найти уравнение кинетической кривой интересующего нас продукта, причем с успехом можно применять численное интегрирование. [9]
На основании предложенного механизма и величин констант скоростей отдельных стадий на ЭВМ были рассчитаны кинетические кривые восстановления СЮ2 и изменения концентраций R2NO и R2NO при различных начальных концентрациях реагентов и рН среды. Они полностью совпадают с экспериментально наблюдаемыми кинетическими кривыми. [10]
Для проверки работоспособности составленной кинетической модели рассчитаны константы скоростей отдельных стадий реакции окисления 3-метилпиридина при различных температурах ( табл.); проведено интегрирование системы. [11]
Для проверки работоспособности составленной кинетической модели рассчитаны константы скоростей отдельных стадий реакции окисления 3-метилпиридина при различных температурах ( табл.); проведено интегрирование системы. [12]
Для выяснения механизма электрохимических реакций и определения констант скорости отдельных стадий может быть использован ряд методов [ например, полярография, производная вольтамперометрия с линейной разверткой потенциала, вольтамперометрия иа дисковом электроде с кольцом ( см. гл. Полученные сведения позволяют осуществлять выбор условий проведения электрохимической реакции. [13]
В рамках этой схемы с использованием известных величин констант скоростей отдельных стадий и величин коэффициентов экс-тинкции было проведено математическое моделирование кинетических кривых изменения оптической плотности. [14]
Если же константа скорости суммарного процесса включает сумму или разности констант скорости отдельных стадий, то уравнение Аррениуса для такого многостадийного процесса может не выполняться. [15]
Страницы: 1 2 3 4