Константа - скорость - второе - порядок
Cтраница 2
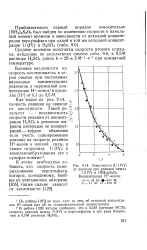 |
Зависимость ( IV. от времени при реакции между. [16] |
Среднее значение константы скорости второго порядка, найденное по результатам опытов табл. 9.6, в 0 5 - М растворе HsSCU равно k 29 3 М-1 ч - 1 при комнатной температуре. [17]
Начальные величины констант скоростей второго порядка при различных концентрациях изоцианата и воды, приведенные в табл. 17, являются достаточно постоянными, что указывает на применимость уравнений второго порядка по крайней мере к начальным стадиям реакции. N-диметилпипера-зин и N-этилморфолин проявляют в 3 - 6 раз меньшую каталитическую активность, чем триэтилендиамин. В бензоле как катализированная, так и некатализированная реакции с водой протекают быстрее, чем в диоксане. В обоих растворителях скорость катализированной реакции с водой составляет около одной трети от скорости соответствующей реакции между фенилизоцианатом и 2-этилгексанолом. [18]
Температурная зависимость константы скорости второго порядка дана ниже. [19]
Константа AS представляет собой нестационарную константу скорости второго порядка. [20]
Константа ks представляет собой нестационарную константу скорости второго порядка. [21]
 |
УФ-спектры геометрических изомеров фенил-р-циан-винилкетона и продукта реакции фенил - ( 3-метокси - [ 3-циан-этилкетона. [22] |
Аналогичным образом была вычислена константа скорости второго порядка для случая г с-фенил - 3-цианвинилкетона, причем измерялось изменение оптической плотности при Я, 270 ммк для первых 20 - 25 % реакции. Ранее мы уже указывали, что г мс-изомер, вероятно, имеет s - tyuc - конформацию, которая не отличается какими-либо значительными пространственными эффектами от / тг / аднс-изомера благодаря небольшим размерам и линейной структуре циангруппы. Найденное незначительное различие в константах скорости для изомеров ( Кг анс 425, К-1 цис 260 л молъ-1 мин-1 при 25 С) может служить подтверждением этого. [23]
Сравнительно большой разброс значений константы скорости второго порядка k объясняется, вероятно, небольшими, но неизбежными изменениями концентрации НС1 в отдельных опытах. [24]
Это отношение объясняет увеличение константы скорости второго порядка k0 с увеличением концентрации спирта. [25]
В табл. 1.1 показана зависимость константы скорости второго порядка как функции катализатора. [26]
 |
Диаграмма энергетических уровней на примере раствора я-аминобензофенона в циклогексане. [27] |
Подставляя значение kg в выражение константы скорости второго порядка k / s, найденной с помощью метода импульсной спектроскопии, можно определить мольный коэффициент экстинкции триплет-триплетных переходов. Кроме этого, одновременное измерение исчезновения S0 дает возможность оценить концентрацию триплетов. [28]
В табл. 15 приведены значения констант скоростей второго порядка ферментативного гидролиза ряда ксилоолиго-сахаридов и в табл. 16 - величины частот расщепления р-ксилозидных связей субстратов под действием эндоксилапазы. [29]
По наклону соответствующих прямых были вычислены константы скорости второго порядка для прямой реакции ( Ki) пръ различных температурах, что позволило в свою очередь рассчитать параметры активации исследуемого превращения. [30]
Страницы: 1 2 3 4