Константа - уравнение - аррениус
Cтраница 1
Константа уравнения Аррениуса для скорости разложения перфторциклобутана равна приблизительно Ю15 сек-1 и лежит в обычных, находимых для мономолекулярных процессов разложения пределах. [1]
Константа уравнения Аррениуса для скорости разложения перфторциклобутана равна приблизительно 1015 сек-1 и лежит в обычных, находимых для мономолекулярных процессов разложения пределах. [2]
Условия термодинамического равновесия позволяют приписать определенное термодинамическое значение константам уравнения Аррениуса, как это только что было продемонстрировано в случае обратимых реакций. [3]
Данная теория делает также попытку обосновать логарифмическую зависимость между константами уравнения Аррениуса, найденную Констеблом, А. А. Баландиным, Швабом и др. Здесь указывается на аналогию с подобной эмпирической закономерностью, существующей для 1электропроводности полупроводников. [4]
Статья Кремер о компенсационном эффекте в гетерогенном катализе интересна главным образом тем, что дает сводку полученного до настоящего времени экспериментального материала по логарифмической зависимости между константами уравнения Аррениуса. [5]
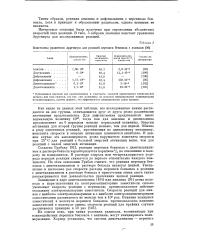 |
Константы уравнения Аррениуса для реакций перекиси бензоила с аминами. [6] |
Интересные сведения были получены при определении абсолютных скоростей этих реакций. В табл. 5 собраны значения констант уравнения Аррениуса для исследованных реакций. [7]
Интересные сведения были получены при определении абсолютных скоростей этих реакций. В табл. 6 собраны значения констант уравнения Аррениуса для исследованных реакций. [8]
I и ранние работы [20-24]) показало, что эта реакция является бимолекулярным гомогенным процессом, имеющим энергию активации порядка 23 - 26 ккал / моль и фактор частоты порядка 1 - Ю10 л / моль-сек. Было установлено, что скорость димеризации мало зависит от природы растворителя и наличия кислых катализаторов; константы уравнения Аррениуса практически одинаковы при проведении реакции в газовой и жидкой фазах. Димеризация замещенных бутадиенов в значительной мере зависит от положения и природы заместителей у диеновой системы. Замещение у средних углеродных атомов цепи бутадиена ( 2 и 3 положения) приводит к увеличению скорости димеризации, а у крайних атомов углерода ( 1 и 4 положения) - к уменьшению ее. [9]
I и ранние работы [20-24]) показало, что эта реакция является бимолекулярным гомогенным процессом, имеющим энергию активации порядка 23 - 26 ккал / моль и фактор частоты порядка ЫО10 л / моль-сек. Было установлено, что скорость димеризации мало зависит от природы растворителя и наличия кислых катализаторов; константы уравнения Аррениуса практически одинаковы при проведении реакции в газовой и жидкой фазах. Димеризация замещенных бутадиенов в значительной мере зависит от положения и природы заместителей у диеновой системы. Замещение у средних углеродных атомов цепи бутадиена ( 2 и 3 положения) приводит к увеличению скорости димеризации, а у крайних атомов углерода ( 1 и 4 положения) - к уменьшению ее. [10]
Одной из необычных особенностей органической химии фтора является часто наблюдаемое образование циклобутанов. Выше было показано, что по сравнению со своими углеводородными аналогами фторуглероды этого типа термодинамически более устойчивы; по-видимому, и скорость образования последних из соответствующих этиленов также больше, чем в случае углеводородов. При изучении кинетики димеризации тетрафтор-этилена и хлортрифторэтилена149 установлено, что процесс является бимолекулярным. В соответствии с бимолекулярными константами скорости энергия активации составляет около 26 ккал / моль а константа уравнения Аррениуса - Ю8 л / моль - сек. [11]
Механизм замещения при насыщенном атоме углерода является основополагающим для химии в целом. Чтобы избежать возможных осложнений при рассмотрении случаев, когда несколько атомов углерода соединены друг с другом, мы ограничимся главным образом реакциями метил - и метиленгалогенидов. Эти процессы идут до конца, не сопровождаются никакими побочными реакциями и являются бимолекулярными. Скорость записанной выше реакции была измерена по убыли алкоголята натрия и накоплению неорганического иодида. Это наблюдение [44] рассеяло весьма распространенное одно время заблуждение, что бимолекулярные реакции идут по простому механизму в газах, но в растворах их механизм, якобы, должен существенно осложняться. Единственное осложнение, которое действительно имеет место в данном случае, состоит в том, что алкоголят натрия в этанольном растворе частично диссоциирует на ионы. Позже мы покажем, что его степень диссоциации при 24 С и концентрации, использованной в описываемых экспериментах, составляет 0 55, и что недиссоциированные молекулы не реагируют с йодистым метилом. Таким образом, реально в растворе идет реакция СН3Ц - С2Н50 - - - СН3ОС2Н5 1 - и надо внести некоторые уточнения в приведенные выше константы уравнения Аррениуса. В процессе обратимого замещения оба метилгало-генида слегка гидролизуются, поэтому проинтегрировать уравнение для скорости реакции не удается. [12]
Страницы: 1