Соответствующая константа - равновесие
Cтраница 1
Соответствующие константы равновесия Л с, A N и Кр связаны друг с другом. [1]
Соответствующие константы равновесия Кс, / и Яр связаны друг с другом. [2]
Соответствующая константа равновесия реакции присоединения второй молекулы ацетилена равна 1 3 0 7 атмт1 при 100 С. [3]
К - соответствующие константы равновесия, выраженные в атмосферах. [4]
Из значений соответствующих констант равновесия вытекают два вывода. Во-первых, равновесная концентрация глицина будет очень близка к 0 0250 М, потому что / Со2 и Къъ очень малы. Во-вторых, рН водных растворов глицина будет меньше 7, так как Kaz для реакции, в результате которой генерируются ионы водорода больше, чем Кь2, для процесса, в результате которого образуются гидроксид-ионы. [5]
Если известны все соответствующие константы равновесия, а также количества присутствующих ионов, можно вычислить соотношение различных ионов, связанных в определенную ионную пару. Результаты таких вычислений для морской воды ( табл. 1) показывают, что образование ионных пар является распространенным явлением. При полном анализе свойств морской воды предполагается, что эти формы должны быть учтены. [6]
Каждое равновесие характеризуется соответствующими константами равновесия / G, Ks, Kis и Ksi. Образование комплекса EIS связано в присоединением ингибитора и субстрата к разным частям молекулы белка, поэтому двойные комплексы EIS и ESI одинаковы. Константы диссоциации Kis и Ksi численно различаются, так как при диссоциации образуются разные продукты EI и I в первом случае и ES и I во втором. Коэффициент р характеризует изменение константы скорости распада комплекса ES в присутствии ингибитора. [7]
Каждое равновесие характеризуется соответствующими константами равновесия Ki, Ks, Kis и Ksi - Образование комплекса EIS связано с присоединением ингибитора и субстрата к разным частям молекулы белка, поэтому двойные комплексы EIS и ESI одинаковы. Константы диссоциации Kis и Ksi численно различны, так как при диссоциации образуются разные продукты: EI и S в первом случае и ES и I во втором. Коэффициент р характеризует изменение константы скорости распада комплекса ES в присутствии ингибитора. [8]
Каждое равновесие характеризуется соответствующими константами равновесия Ki, Ks, Kis, и / Csi. Образование комплекса EIS связано в присоединением ингибитора и субстрата к разным частям молекулы белка, поэтому двойные комплексы EIS и ESI одинаковы. Константы диссоциации / Cis и / Csi численно различаются, так как при диссоциации образуются разные продукты EI и I в первом случае и ES и I во втором. Коэффициент ( 3 характеризует изменение константы скорости распада комплекса ES в присутствии ингибитора. [9]
Там же приведены и соответствующие константы равновесий. [10]
Там же приведены и соответствующие константы равновесий. [11]
Зависимость скорости реакции от соответствующей константы равновесия является общей особенностью полученных формул: большим значениям Кр соответствуют большие скорости взаимодействия. [12]
Для некоторых фенолов были измерены соответствующие константы равновесия. Оказалось, что для R-трет. [13]
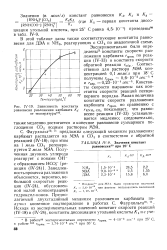 |
Значения констант равновесия80 при 20 С.| Зависимость константы карбоната гпрям. по сравнению с. [14] |
В этой таблице даны также соответствующие константы равновесия для ДЭА и NH3, реагирующих с СО2 по аналогичной схеме. [15]
Страницы: 1 2 3 4