Измеренная константа - равновесие
Cтраница 1
Измеренные константы равновесия, хотя и являются концентрационными, не зависят от концентраций разных ионов, так как при постоянной ионной силе в условиях избытка NaClO4 коэффициенты активности постоянны. [1]
Важно иметь в виду, что любая измеренная константа равновесия ком-плексообразования в растворе фактически представляет собой сумму констант равновесия образования всех возможных комплексов стехиометрии 1: 1 и только в том случае, когда один из этих комплексов гораздо устойчивее, чем все остальные, наблюдаемая константа равновесия будет равна константе устойчивости соответствующего комплекса. Следовательно, наблюдаемая константа равновесия комплексообразования в растворе может быть больше константы устойчивости комплекса, в котором возникает полоса поглощения переноса заряда, если одновременно образуются и другие комплексы, в которых эта полоса отсутствует. Такая ситуация особенно вероятна в случае, когда энергия образования КПЗ мала, что бывает довольно часто. Если только часть образующихся комплексов обладает поглощением переноса заряда, экспериментально найденный коэффициент экстинкции будет занижен, так как он будет усреднен по всем образующимся комплексам. Фактически при очень слабых взаимодействиях почти все наблюдаемое поглощение переноса заряда может быть обусловлено скорее контактным переносом заряда, чем образованием КПЗ. Это проявляется в непостоянстве экспериментально установленного коэффициента экстинкции комплекса в различных условиях в зависимости от доли поглощающих комплексов. [2]
Используя вычисленные ими значения термодинамических функций компонентов реакции и измеренные константы равновесия реакции ( XXVIII. Расчет с использованием принятых в Справочнике значений термодинамических функций привел к АЯ0 87 3 ккал / моль и ЛЯ % ЮН газ) - 55 6 ккал / моль. [3]
Нередко приходится встречаться и с обратной задачей, когда по экспериментально измеренным константам равновесия химических реакций надо найти термохимические величины AG, АЯ или AS реакции. [4]
В очень редких случаях значения энтальпии и энтропии получены из температурной зависимости измеренных констант равновесия. Такие данные отмечены буковй F перед соответствующей литературной ссылкой. [5]
III уравнение Вант-Гоффа было проинтегрировано и применено для определения энтальпии реакции с помощью измеренных констант равновесия. Первые два метода, рассмотренные в этой главе, могут быть использованы для расчета констант равновесия по данным энтальпии реакции при условии, если известно экспериментальное значение константы равновесия при какой-либо одной температуре. Поскольку в таких расчетах используются только изменения энтальпий и энтропии реакций и не используются абсолютные значения энтропии участвующих в них веществ, эти два метода обычно называют методами определения термодинамических свойств по второму закону термодинамики. [6]
Из уравнения ( 17), для которого постоянная интегрирования вычислена на основании измеренных констант равновесия, AG298 - 3910 кал / моль. Таким образом, оба значения AG достаточно близки. [7]
Важность этого простого соотношения обусловлена тем, что значения энтальпии реакции ДЯГ можно вычислять по экспериментально измеренным константам равновесия КР. [8]
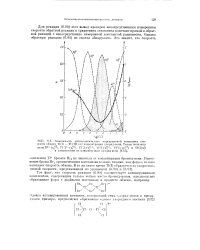 |
Зависимость экспериментально определяемой копстанты скорости обмена П ( Т - Т1 ( III от концентрации хлорид-попа. Также показаны. [9] |
Для реакции (6.90) этот вывод проверен непосредственным измерением скорости обратной реакции и сравнением отношения констант прямой и обратной реакций с непосредственно измеренной константой равновесия. [10]
Эти вычисления показали, что при изменении температуры от 1735 ( I 5 мм) до 1304 К ( I 85 мм) измеренная константа равновесия ( в отличие константы Кт), как и парциальные давления четырех газов, в пределах погрешности измерений остается неизменной. Отсюда следует, что вблизи внутреннего пламени в междуконусном газе устанавливается равновесие, как это было найдено и в опытах [ 9011, которое не смещается при понижении температуры. В работе [136] при помощи кинетических уравнений были оценены относительные парциальные давления Н, ОН и СН3 и было показано, что главным химическим процессом в зоне сгоревших газов является рекомбинация этих частиц. Заметим, что наблюдаемая в этих опытах закалка равновесия, несмотря на наличие активных частиц, подтверждает сделанное выше заключение о слабом влиянии этих частиц ( ввиду их относительно малой концентрации) на химическое равновесие в зоне сгоревших газов. [11]
В табл. 23 на основе данных, приводимых в [36], сопоставлены значения ДЯ и Д5, определенные но данным стандартных термодинамических таблиц и по экспериментально измеренным константам равновесия для газофазной изомеризации парафиновых и ароматических углеводородов. [12]
По термодинамике синтеза метанола уже до 1930 г. было опубликовано сравнительно большое число расчетно-теоретических работ [13 - 17], однако они здесь не разбираются, так как в основу их были положены неточные термохимические данные; результаты этих расчетов в большинстве случаев значительно отличаются от экспериментально измеренных констант равновесия и поэтому не представляют в настоящее время большого интереса. [13]
Расчет изменений стандартной свободной энергии на основании измерения константы равновесия и уравнения (11.22) на первый взгляд не является тривиальным. Для реакций, включающих отщепление или присоединение протона ( весьма обычных в биохимических процессах), такие расчеты могут быть выполнены тремя разными способами, причем все три способа правильны. Первой измеренной константой равновесия была константа равновесия реакции гидролиза этилацетата, определенная Бертло и Гиле-сом в 1863 г. На примере этой реакции можно рассмотреть все три способа, используемых для подсчета изменений стандартной свободной энергии. [14]
Коэффициент экстинкции иода, измеряемый при данной длине волны, также нечувствителен к температуре. При расчете АЯ по уравнению ( 20) предпочтительно использовать не сами константы равновесия, а наклон прямой, так как наклоны [ / ( ( EDA - еА) ] - можно определить значительно более точно, чем значения К. Если в растворах донора и акцептора присутствует несколько типов комплекса 1: 1, включая контактные комплексы с переносом заряда, величина АЯ; рассчитанная по измеренным константам равновесия К, должна зависеть от температуры, если только все компоненты не имеют одинаковых теплот образования. [15]
Страницы: 1 2