Кажущаяся константа - устойчивость
Cтраница 1
Кажущаяся константа устойчивости показывает отношение между концентрациями связанного в комплекс и свободного иона металла при каждой данной концентрации комплексов бра-зующего вещества. Это отношение меняется при меньших концентрациях комплексообразующего вещества в пользу свободного иона металла ( или аквакомплекса), при более высоких концентрациях - в пользу комплекса. [1]
Большие значения кажущихся констант устойчивости, определенные с помощью уравнений вида (IV.71) из полярографических волн, полученных с постоянным и переменным током, объясняют [183, 191 ] присутствием на поверхности ртути специфически адсорбированных комплексов, восстановление которых затруднено по сравнению с восстановлением специфически не взаимодействующих с ртутью комплексов. [2]
Смх называется кажущейся константой устойчивости комплекса. [3]
При любых данных условиях эксперимента кажущиеся константы устойчивости комплексов ряда металлов изменяются в порядке, который зависит от природы лиганда. Так, EDTA образует с Са2 более прочные комплексы, чем с Mg2, а в случае эриохром черного Т наблюдается обратный порядок и константа устойчивости комплекса Са2 слишком мала, чтобы титрование было удовлетворительным. Добавление к раствору небольших количеств комплекса Mg-EDTA приводит к четкой конечной точке. До тех пор пока в растворе остается какое-то количество незакомплексованного Са2, в нем будет находиться свободный Mg2, образующий с индикатором окрашенный комплекс. Однако комплекс Mg-EDTA достаточно устойчив, и в тот момент, когда он снова образуется, окраска раствора исчезает. Комплекс Mg-EDTA служит примером косвенного металлиндикатора. Применение этого принципа имеет богатые потенциальные возможности. [4]
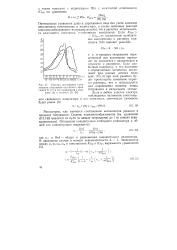 |
Спектры поглощения комп лексных соединений кислотного хром синего К ( 1 и его комплексов с каль цием ( 2 и магнием ( 3. [5] |
Приведенные уравнения даны в упрощенном виде без учета констант диссоциации комплексона и индикатора, а также побочных реакций комплексообразования, но предполагается, что в расчетах используются кажущиеся константы устойчивости комплексов. [6]
Химические свойства кадмия и цинка очень близки, поэтому оба элемента можно определить по одной методике. В этом случае кажущиеся константы устойчивости достаточно сильно различаются, чтобы можно было проводить фотометрическое титрование ( стр. [7]
Различия в значениях log / Ci для комплексов Си, Ni и Fe с TREN достаточно велики, что позволяет последовательно титровать эти металлы в одном растворе. Кроме того, чтобы получить достаточно большие кажущиеся константы устойчивости, определения - вследствие неблагоприятных значений рДа лигандов - надо проводить в слабощелочной среде. [8]
Количественной характеристикой устойчивости любого комплексного соединения ЛЩ является его термодинамическая константа устойчивости р амкя / Ома. В аналитической практике для количественной оценки устойчивости соединений часто пользуются также концентрационными или кажущимися константами устойчивости PMR [ MRn3 / [ M ] [ R ] ( в квадратных скобках указаны равновесные концентрации окрашенного комплекса, определяемого катиона М и реагента R), зависящими не только от температуры, но и от ионной силы раствора. [9]
Так как активность бикарбонат-иона находится в обратной зависимости от рН, в этом выражении должна быть отражена зависимость кажущейся константы от четвертой степени концентрации ионов водорода, при которой исследовалось равновесие, и прямая зависимость от парциального давления двуокиси углерода в атмосфере, в равновесии с которой они находятся. Из величин, которые используются для количественного описания связывания металлов с трансферрином, по-видимому, наиболее важны с точки зрения физиологии кажущиеся константы устойчивости. [10]
При наличии окислительно-восстановительных процессов применяют окислительно-восстановительные индикаторы или определяют точку эквивалентности инструментальными методами. Как только прореагирует эквивалентное количество комплексов с ионами Fe3, значение pFe для железа ( III) скачкообразно повышается, а окислительно-восстановительный потенциал резко падает. При этой кислотности ионы Fe2 даже при значительном избытке ЭДТА остаются в растворе, так как кажущаяся константа устойчивости комплексоната железа ( II) FeY2 - незначительна. Железо ( II) при рН7 образует гидрокомплексы в растворе, в котором кроме ОН ионов не имеется других комплексообразующих анионов. [11]
При наличии окислительно-восстановительных процессов применяют окислительно-восстановительные индикаторы или определяют точку эквивалентности инструментальными методами. Например, если титровать смесь Fe2 - и Ре3 - ионов раствором ЭДТА, то в первую очередь вступают во взаимодействие Ре3 - ионы. Как только прореагирует эквивалентное количество комплексона с Ре3 - ионами, значение pFe для железа ( III) скачкообразно повышается, а окислительно-восстановительный потенциал резко падает. При этой кислотности Ре2 - ионы даже при значительном избытке ЭДТА остаются в растворе, так как кажущаяся константа устойчивости комплексоната железа ( II) - FeY2 - незначительна. Железо ( II) при рН 7 образует гидрокомплексы в растворе, в котором кроме ОН - - ионов не имеется других комплексоабразующих анионов. [12]
Страницы: 1