Термодинамическая константа - диссоциация
Cтраница 3
Как видно из табл. XVIII, 1, значения термодинамических констант диссоциации слабых кислот, растворенных в воде, проходят через максимум, который для приведенных в таблице кислот лежит в интервале между 0 и 60 С. [31]
Кно истинная термодинамическая константа диссоциации уксусной кислоты равна ее термодинамической константе диссоциации. Это, конечно, остается верным и для истинных термодинамических констант диссоциации всех других кислот при рассмотрении их диссоциации в водной среде. [32]
Эти константы, как указано выше, численно равны соответствующим термодинамическим константам диссоциации. [33]
Сн 0 истинная термодинамическая константа диссоциации уксусной кислоты равна ее термодинамической константе диссоциации. Это, конечно, остается верным и для истинных термодинамических констант диссоциации всех других кислот при рассмотрении их диссоциации в водной среде. В табл. XVIII, 3 приведены константы диссоциации различных соединений, способных отщеплять протон. [34]
Величину / Сд, в том случае, если, берутся активности, называют термодинамической константой диссоциации, а при использовании значений, принятых в формуле (1.5), - константой диссоциации. Уравнение (1.5) выражает закон разведения Оствальда; он связывает константу диссоциации со степенью диссоциации электролита. Очевидно, что чем больше / Сд, тем выше степень диссоциации. Таким образом, величина / Сд может служить мерой силы кислоты. [35]
Константу диссоциации, определяемую через активности по ( XII, 2), нередко называют термодинамической константой диссоциации. Практически, однако, при отсутствии данных об активности часто приходится и для сравнительно концентрированных растворов пользоваться соотношением ( XII. Рассчитанная таким способом / Сд может несколько изменяться с концентрацией. Ее называют иногда условной константой диссоциации. [36]
Константу диссоциации, определяемую через активности по ( XII, 2), нередко называют термодинамической константой диссоциации. Рассчитанная таким способом / Сд может несколько изменяться с концентрацией. Ее называют иногда условной константой диссоциации. [37]
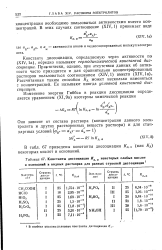 |
Константы диссоциации Кя а некоторых слабых кислот и оснований в водных растворах для разных ступеней диссоциации. [38] |
Константу диссоциации, определяемую через активности по ( XIV, 1а), нередко называют термодинамической константой диссоциации. Практически, однако, при отсутствии данных об активности часто приходится и для сравнительно концентрированных растворов пользоваться соотношением ( XIV. Рассчитанная таким способом Кя может несколько изменяться с концентрацией. Ее называют иногда условной константой диссоциации. [39]
Здесь Кс 0 13 - концентрационная константа диссоциации трихлоруксусной кислоты) и Ка 3 2 - Ю-7 - термодинамическая константа Диссоциации гидрохромат-иона. [40]
В растворе устанавливается равновесие, константа которого равна отношению истинных термодинамических констант диссоциации или, что то же самое, отношению термодинамических констант диссоциации Кя. [41]
Экстраполяция на / 0 с помощью или без помощи приближенных коэффициентов активности, вычисленных по уравнению Дебая и Хюк-келя, дает термодинамическую константу диссоциации К. Лучшее значение стандартного потенциала, по-видимому, то, которое дает величину рН, согласующуюся с известным значением константы диссоциации. [42]
Обычно коэфициенты активности оказывают очень небольшое влияние на результат ( см. задачу 348), поэтому во многих случаях можно производить расчеты по термодинамическим константам диссоциации как по концентрационным константам. [43]
Обычио коэффициенты активности оказывают очень небольшое влияние на результат ( см. задачу 340), поэтому во многих случаях можно производить расчеты по термодинамическим константам диссоциации как по концентрационным константам. [44]
Термодинамические константы диссоциации уксусной и хлоруксусной кислот равны 1 75 - 10 - 5 и 1 38 - 10 3 соответственно. [45]
Страницы: 1 2 3 4