Критическая константа
Cтраница 2
Для определения различных критических констант были использованы образцы, описанные выше. [16]
Эти значения представляют собой критические константы газа, выраженные через коэффициенты а и b уравнения Ван-дер - Ваальса. [17]
Полученные значения представляют собой критические константы газа, выраженные через коэффициенты а и b уравнения Ван-дер - Ваальса. [18]
Экспериментально найденные значения критических констант приводятся в справочной литературе. В связи с тем, что опытных данных имеется мало, были предложены различные расчетные методы, основанные на обработке опытных данных. Число предложенных эмпирических уравнений очень велико. [19]
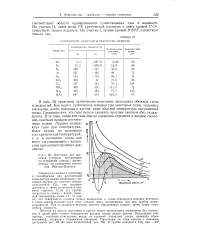 |
Изотермы для двуокиси углерода, построенные на основании данных, вычисленных по уравнению состояния Ван-дер - Ваальса. [20] |
В табл. 22 приведены критические константы нескольких обычных газов и жидкостей. Как видим, критические температуры некоторых газов, например кислорода, азота, водорода и аргона, ниже обычной температуры окружающей среды. В те годы, когда эти газы еще не удавалось перевести в жидкое состояние, они были названы постоянными газами. [21]
В настоящее время известны критические константы для многих веществ, определенные опытным путем и помещенные в соответствующих справочниках. Однако представляет интерес ознакомиться и с некоторыми эмпирическими формулами расчета критических параметров. [22]
Исходя из известных значений критических констант, он смог при помощи этой формулы установить для некоторых газов значение величины d ( pv) / dp и при помощи соотношений, выведенных на основании фиг. [23]
 |
Экспериментальные и вычисленные значения pV для этилена при 293 К. [24] |
Явление конденсации и существование критических констант характерны для реальных газов. [25]
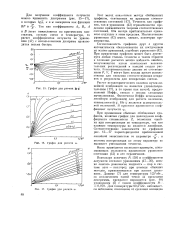 |
График для расчета lg у.| График для расчета и.| График для расчета w. [26] |
В легко вычисляются по критическим константам, составу смеси и температуре, то расчет коэффициентов летучести по уравнению ( 47) с использованием диаграмм производится весьма быстро. [27]
Марчман и соавторы [94] изучили критические константы пропена и давление насыщенного пара его при трех температурах. Высокая чистота исходного пропена подтверждалась постоянством давления при изменении объема от состояния насыщенного пара до насыщенной жидкости. [28]
Для пользования графиком необходимо знать критические константы нефтепродукта и молекулярный вес. [29]
При отсутствии в литературе значений критических констант, необходимых для определения величины Р, они могут быть рассчитаны по формулам, приводимым в курсах химической термодинамики и физической химии. [30]
Страницы: 1 2 3 4