Высокая константа - равновесие
Cтраница 1
 |
Совместное окисление пропилена и ацетальдегида, растворенных в бензоле, при 70 С и 5 МПа. [1] |
Высокая константа равновесия указывает на большую вероятность реакции 10, и эта реакция становится основным путем превращения ацильных перекисных радикалов, конкурируя с соответствующими реакциями в гомогенных условиях. Невысокие концентрации СО2 ( табл. 111) указывают, что реакция 10 протекает главным образом гетерогвнно, без выхода радикалов в объеме раствора, так как в противном случае, согласно реакции 5, образовывалась бы двуокись углерода. [2]
При этом стадия I проходит с высокой константой равновесия, тогда как стадия II с низкой константой равновесия. [3]
Реакция обратима и эндотермична, поэтому для достижения высокой константы равновесия требуется высокая температура, однако выше 650 С выход стирола падает из-за более глубокой деструкции субстрата. [4]
В отличие от реакций в жидкой фазе парофазная этерификация карбоновых кислот спиртами является экзотермической и имеет более высокую константу равновесия, зависящую от температуры. Так, при получении этилацетата в паровой фазе она равна 30 при 150 С и 9 при 300 С. [5]
Вместе с тем, если для реакции 1 2-цис - - 1 2-транс характерно выделение тепла и высокая константа равновесия, то для аналогичной реакции 1 3-диалкилзамещенных - поглощение тепла и низкая константа равновесия. [6]
В отличие от реакций в жидкой фазе, газофазная этерифи-кация карбоновых кислот спиртами является экзотермической и имеет более высокую константу равновесия, зависящую от температуры. Так, при получении этилацетата в газовой фазе константа равновесия равна 30 при 150 С и 9 при 300 С. [7]
Предполагается [63], что при взаимодействии иодида серебра с концентрированным раствором KI образуется комплексный ион Ag2Ie, из которого при электролизе катодно восстанавливается серебро по суммарной реакции: Ag2Ie - 2e 2Ag 6I -, причем лимитирующей стадией на этом этапе является диффузия комплексных ионов. Благодаря высокой константе равновесия реакции, в иодидном электролите при загрузке деталей в ванну под током не требуется проводить предварительного серебрения или амальгамирования для меди и ее сплавов. С понижением рН путем введения кислоты повышается стойкость серебряного комплекса, но несколько снижается катодный выход металла по току. [8]
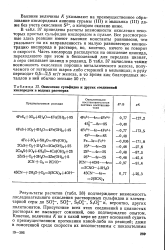 |
Окисление сульфидов и других соединений кислородом в водных растворах. [9] |
В табл. 37 приведены расчеты возможности окисления некоторых простых сульфидов кислородом в пульпе. Все рассмотренные здесь реакции имеют высокие константы равновесия, что указывает на их направленность и малую равновесную концентрацию кислорода в растворе, но, конечно, ничего не говорит о скорости. Часть кислорода расходуется на окисление цианида, переходящего при этом в бесполезный для передела цианат, а сера связывает цианид в роданид. [10]
Шс-1 2-харак-терны выделение тепла и высокая константа равновесия, то для аналогичной реакции 1 3-диалкилзамещенных характерны поглощение тепла и низкая константа равновесия. [11]
В качестве основания В может выступать не только растворитель, но и любое нейтральное основание, сильное или слабое. Сильные основания В взаимодействуют легко, быстро, с высокой константой равновесия реакции (5.4) и сильно отрицательной энтальпией. Поскольку в реакции (5.4) из двух незаряженных частиц образуется два носителя заряда, способные к сильному ион-дипольному взаимодействию (5.7) с растворителем, как правило, общее число частиц сильно уменьшается, что приводит к отрицательной энтропии ( - AS) для таких реакций. [12]
 |
Сигмоидная кинетическая кривая насыщения субстратом. [13] |
К ферментам применимы три основных критерия, характерных и для неорганических катализаторов. Катализаторы лишь повышают скорость, с которой система приближается к термодинамическому равновесию, не сдвигая точки равновесия. Химические реакции с высокой константой равновесия и отрицательной величиной AG принято называть экзергоническими. Реакции с низкой константой равновесия и соответственно положительной величиной AG ( они обычно не протекают спонтанно) называются эндерго-ническими. [14]
Закись железа ( FeO) ниже 560 является нестабильной фазой. Восстановление окиси железа ( Гел03) в магнетит ( для которого данные не приведены характеризуется более высокими константами равновесия и термодинамически более вероятно, чем восстановление магнетита в железо. Восстановление окисей металлов окисью углерода или газом синтеза может осложняться образованием свободного углерода и карбидов. Константы равновесия восстановления окисей кобальта и никеля достаточно велики, так что металл является устойчивой объемной фазой при равновесии с газами, обычно присутствующими в ходе синтеза. [15]
Страницы: 1