Рассчитанная константа - равновесие
Cтраница 1
Рассчитанные константы равновесия для циклогексана, изоок-тана и четыреххлористого углерода близки к константам, полученным Редлихом, что доказывает, что процессы доведены до равновесия. Константы равновесия для декалина и хлороформа, отсутствующие в известной нам литературе, дают возможность судить о выходе комплекса при данных процессах. [1]
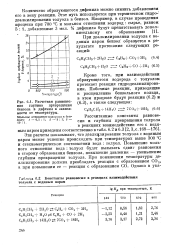 |
Расчетная равновесная глубина превращения бензола в дифенил в зависимости от температуры.| Константы равновесия в реакциях взаимодействия толуола с водяным паром. [2] |
Рассчитанные константы равновесия и глубины превращения толуола в реакциях взаимодействия его с водяным паром приведены соответственно в табл. 6.2 и 6.3 [ 2 3, с. Эти расчеты показывают, что деалкилирование толуола с водяным паром может успешно происходить при температурах выше 300 С и стехиометрическом соотношении вода: толуол. [3]
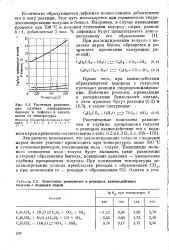 |
Расчетная равновесная глубина превращения бензола в дифенил в зависимости от-температуры.| Константы равновесия в реакциях взаимодействия толуола с водяным паром. [4] |
Рассчитанные константы равновесия и глубины превращения толуола в реакциях взаимодействия его с водяным паром приведены соответственно в табл. 6.2 и 6.3 [ 2 3, с. С и стехиометрическ ом соотношении вода: толуол. [5]
До настоящего времени не было сообщений о присутствии в продуктах изомеризации 2 2-диметилпропана, который соответственно рассчитанным константам равновесия должен бы быть одним из главных компонентов при изомеризации пентанов при комнатной температуре. [6]
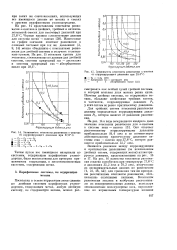 |
Зависимость константы равновесия в-пентана от коррелирующего давления при 37 8 С.| Зависимость константы равновесия н-пентана от коррелирующего давления при 29 4 С. [7] |
На рис. 16 нанесены константы равновесия этилена и изобутана при температуре 37 8 С и давлениях 35 2 ата и 70 3 ата, полученные из экспериментальных данных по равновесию [1, 21, 26, 44]; для сравнения там же приведены рассчитанные константы равновесия, обозначенные сплошными линиями. [8]
Полученные величины коэффициентов активности твердой фазы сильно зависят от молярной доли компонента в смоле, причем для трех рассмотренных концентраций раствора не совпадают между собой, хотя и близки друг к другу. Рассчитанные константы равновесия равны соответственно 1 73 для 1 М, 1 68 для 0 3 М и 1 66 для 0 1 М растворов. [9]
Совпадение расчета с экспериментом было недостаточно удовлетворительным. Рассчитанные константы равновесия метана были приблизительно на 5 % выше экспериментальных значений, в то время как для азота константы были примерно на 15 % ниже. [10]
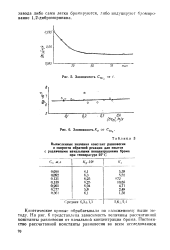 |
Зависимость СВг от t.| Зависимость Кр от. [11] |
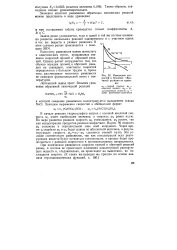
На рис. 6 представлена зависимость величины рассчитанной константы равновесия от начальной концентрации брома. [12]
Поэтому трудно представить метод, используя который можно было бы проверить рассчитанные константы равновесия между цис - и грй с-формами. Положение несколько отлично для аналогичных систем комплексов кобальта ( III) и хрома ( III), где можно, вследствие инертности отдельных комплексов, приготовить различные изомеры в чистом виде. [13]
Поэтому трудно представить метод, используя который можно было бы проверить рассчитанные константы равновесия между цис - и транс-формами. [14]
 |
Изменение ско. [15] |
Страницы: 1 2