Криоскопическая константа - растворитель
Cтраница 1
Эбуллиоскопические и криоскопические константы растворителя ( табл. 7) определяют, исходя из экспериментальных ДаННЫХ ПО А / кип И А / зам ДЛЯ рЗСТВОрОВ С ЗЯ-ранее известной моляльной концентрацией. [1]
Эбуллиоскопические и криоскопические константы растворителя определяют, исходя из эксперименталы ных данных. [2]
К - криоскопическая константа растворителя, численно равная понижению его температуры плавления ( в С) в результате растворения 1 моль вещества в 1000 г растворителя; С - концентрация растворенного вещества ( в г на 1000 г растворителя); М - масса 1 моль растворенного вещества. [3]
К - эбулиоскопическая или криоскопическая константа растворителя. [4]
К - эбулиоскопическая или криоскопическая константа растворителя. [5]
Постоянная прибора связана с криоскопической константой растворителя. [6]
ДГзам - понижение температуры замерзания; Кк - криоскопическая константа растворителя или моляльное понижение температуры замерзания; т - концентрация раствора, выраженная в молях растворенного вещества на 1000 г растворителя. [7]
АТзам - понижение температуры замерзания; Кк - криоскопическая константа растворителя или молялыюе понижение температуры замерзания; т - концентрация раствора, выраженная в молях растворенного вещества па 1000 г растворителя. [8]
Концентрацию воды в пробе рассчитывали по формуле CH о ( 2 - ti) M / K, где М - молекулярная масса воды; К - криоскопическая константа растворителя, равная 5 12 для бензола и 20 2 для циклогексана. [9]
Концентрацию воды в пробе рассчитывали по формуле Сн о ( 2 - ti) M / K, где М - молекулярная масса воды; К - криоскопическая константа растворителя, равная 5 12 для бензола и 20 2 для циклогексана. [10]
Найти молекулярную массу растворенного вещества эбулиоскопическим или криоскопинеским методом - это значит найти такое количество граммов его, которое, будучи растворено в 1000 г растворителя, повысит температуру кипения раствора на величину, равную эбулиоскопи-ческой константе растворителя, или соответственно понизит температуру кристаллизации раствора на величину, равную криоскопической константе растворителя. [11]
Найти молекулярную массу растворенного вещества эбулиоско-пическим или криоскопическим методом - это значит найти такое количество его ( в граммах), которое, будучи растворено в 1000 г растворителя, повысит температуру кипения раствора на величину, равную эбулиоскопической константе растворителя, или соответственно понизит температуру кристаллизации раствора на величину, равную криоскопической константе растворителя. [12]
Понижение точки замерзания, вызываемое ( по рас чету) растворением одного моля вещества в 1000 г рас творителя, есть величина постоянная для данного растворителя. Она называется криоскопической константой растворителя. Точно так же и повышение точки кипения, вызываемое растворением одного моля вещества в 1000 г растворителя, является постоянной величиной и называется эбулиоскопической константой растворителя. Для разных растворителей криоскопические и эбу лиоскопические константы различны. [13]
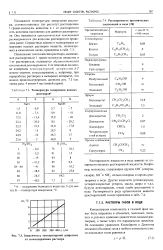 |
Температура замерзания водных растворов.| Растворимость органических соединений в воде. [14] |
Понижение температуры замерзания раствора, соответствующее ( по расчету) растворению 1 грамм-молекулы вещества в 1 кг растворителя есть величина постоянная для данного растворителя. Она называется криоскопической константой растворителя и для воды как растворителя приведена ранее. [15]
Страницы: 1 2