Равновесная константа
Cтраница 1
Равновесная константа в этом случае больше при более низких температурах, причем катализатор должен быть селективным, чтобы избежать горения. [1]
Равновесные константы образования тридентатного бората, зависящие от наличия в молекулах несвязанных взаимодействий, позволяют рассчитать значения энергий этих взаимодействий. Для этого необходимо сделать два допущения. Строго говоря, ни одно из этих утверждений не является верным, однако принимая их, мы вносим, очевидно, лишь незначительную погрешность. [2]
Если равновесная константа образования ( E-S) из E-S совпадает с константой образования S0 из S0 в отсутствие комплекс ообразующего агента, то в присутствии последнего скорость реакции не будет увеличиваться. [3]
Величины равновесных констант для комплексо-образования Ри4 ( и РиО) с хлорид-ионом ( а также с нитрат-и сульфат-ионами) получены на основании влияния этих анионов на окислительно-восстановительные потенциалы пар. Эта работа выполнена тщательно и подробно. Так как влияние комплексо-образования на величину измеряемого формального потенциала указывает только на различие в устойчивости комплексных ионов, степень связи в комплекс одного из ионов должна быть определена независимым методом. Так было сделано при исследовании ком-плексообразования плутонил-иона с хлоридами. [4]
Аналогичные формулы для равновесной константы могут быть написаны и для других экстрагируемых соединений. Из этих отношений очевидно, что коэффициент распределения зависит как от концентрации нитрата в водной фазе, так и от содержания ТБФ в органической фазе. [5]
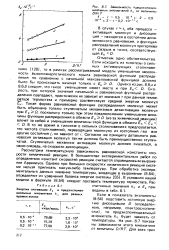 |
Зависимость предэкспонен-циальных множителей ka от величины D / R Г. [6] |
Рассмотрим температурную зависимость равновесной константы скорости химической реакции. В большинстве экспериментальных работ по определению констант скоростей реакции считается справедливым выражение Аррениуса. [7]
Катц допускает, что равновесная константа гидратообразования К для к-бутана такая же, как и для этана, если концентрация последнего невелика. Константа К для азота и тяжелых углеводородов неопределенна, так как они или вообще не образуют гидратов или образуют их с большим трудом. [8]
Предположения о невозможности использования равновесных констант, а следовательно, и перечисленных выше уравнений для оценки выбора избирательных растворителей нуждаются в дополнительных исследованиях. Правда, степень растворения - понятие кинетическое, так как оно характеризует величину растворения соединения не вообще при данных условиях, а за произвольный промежуток времени. Однако нет причин сомневаться в том, что существует некоторая пропорциональность, например, между величиной растворимости и весовым количеством растворяющегося за определенный промежуток времени соединения. Подобная пропорциональность, несомненно, имеется также между величиной константы нестойкости и весовыми количествами ионов, образующих комплексное соединение за тот же промежуток времени. [9]
В табл. 4.15 приведены значения равновесных констант экстракции Кэ и констант Диссоциативного равновесия Кд, измеренных Френсдорфом [ 238] для нескольких систем. Значение константы экстракции Кэ зависит от константы устойчивости ( К) комплекса в водном растворе и коэффициента распределения краун-эфира и комплекса; при этом решающим оказывается значение коэффициента распределения комплекса. [10]
В табл. 4.15 приведены значения равновесных констант экстракции Кэ и констант Диссоциативного равновесия Кд, измеренных Френсдорфом [ 238] для нескольких систем. Значение константы экстракции Кэ зависит от константы устойчивости ( К) комплекса в водном растворе и коэффициента распределения краун-эфира и комплекса; при этом решающим оказывается значение коэффициента распределения комплекса. [11]
Экспериментальное значение ( К) равновесной константы диссоциации комплекса C-S эквивалентно такой концентрации субстрата, при которой скорость реакции равна половине максимальной. Константа скорости & кат является максимальной константой скорости. [12]
 |
Условия гидратообразования для ие-углевюдородных газов.| Условия гидратообразоваяия природных газов [ V. 21, , V. 42 ].| Условия гидратообразования при. [13] |
Для азота и углеводородов тяжелее бутана равновесные константы берутся как бесконечность, так как они затрудняют образование смешанных гидратов. Константы равновесия принимаются как функция только давления и температуры, но фактически они зависят и от состава газа. [14]
Превышение множителя Л в выражении для равновесной константы над числом столкновений можно объяснить, во-первых, теми же факторами, которые определяют ее превышение над неравновесной константой, и, во-вторых, влиянием таких факторов, как вращение молекулы [2146], наличие нескольких устойчивых электронных состояний [1067] и увеличение поперечника молекулы при возбуждении колебаний. [15]
Страницы: 1 2 3 4