Дополнительные доказательства
Cтраница 1
Дополнительные доказательства, подтвердившие нахождение двойной связи в положении 5 6, были получены Хейльброном292 в процессе дальнейшего исследования. [1]
Дополнительные доказательства в пользу предположения о том, что преимущественно подвергаются расщеплению наиболее циклические молекулы и что это предположение особенно справедливо в случае более сложных кольцевых систем высокомолекулярных фракций перерабатываемого сырья, были получены на основании анализа фракций, выделенных перегонкой гидрированного смазочного масла в высоком вакууме. В табл. 95 приводятся свойства и распределение углерода для ряда таких фракций, перегнанных в высоком вакууме и расположенных в порядке возрастания молекулярного веса. Из этих данных видно, что содержание колец в фракциях понижается с увеличением молекулярного веса. [2]
Дополнительные доказательства в поддержку этой реакции были получены при измерении концентрации водородных ионов, которая изменяется с изменением концентрации уранил-иона. [3]
Дополнительные доказательства этого были получены при сравнении скоростей сольволиза вторичных и третичных систем. При сольволизе в 80 % - ном этиловом спирте переход от изопро-пилбромида к грет-бутилбромиду приводит к увеличению скорости сольволиза в 1035 раз. Изменение скорости при переходе от вторичного бромида к третичному связано с увеличением стабильности образующегося катиона ( или ионной пары) за счет электронодонорных свойств метильной группы. Однако одновременно происходит уменьшение нуклеофильного содействия, которое в третичных системах невозможно по стерическим причинам. В 2-бром-адамантильной системе стерические взаимодействия также приводят к тому, что нуклеофильное содействие растворителя не проявляется, и отношение скоростей определяется относительной стабильностью переходных состояний, близких по строению к карбкатиону. В то же время в изопропильной системе возможно значительное нуклеофильное содействие растворителя, которое приводит к понижению энергии переходного состояния. Этим и объясняется тот факт, что при переходе от изопропилбро-мида к грег-бутилбромиду увеличение скорости значительно меньше. [4]
Дополнительные доказательства были получены из инфракрасных спектров тех же твердых веществ. Наблюдать спектры комбинационного рассеяния Н3О более ложно. [5]
Дополнительные доказательства в пользу предположения о том, что преимущественно подвергаются расщеплению наиболее циклические молекулы и что это предположение особенно справедливо в случае более сложных кольцевых систем высокомолекулярных фракций перерабатываемого сырья, были получены на основании анализа фракций, выделенных перегонкой гидрированного смазочного масла в высоком вакууме. В табл. 95 приводятся свойства и распределение углерода для ряда таких фракций, перегнанных в высоком вакууме и расположенных в порядке возрастания молекулярного веса. Из этих данных видно, что содержание колец в фракциях понижается с увеличением молекулярного веса. Величины показателей преломления и плотностей также уменьшаются, что редко наблюдается в смазочных маслах и что указывает на селективное удаление высокоцикличных соединений из тяжелых фракций. [6]
Дополнительные доказательства справедливости этих формул получены из данных по измерению мольной электропроводности, которые показывают, что в перечисленном порядке вещества представляют собой один-три -, один-два - и один-один-зарядные электролиты. [7]
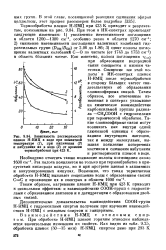 |
Зависимость растворимости пленок Н - КМЦ в воде при комнатной температуре ( 7, при кипячении ( 2 и набухания их в воде ( 3 от времени термообработки при 423 К. [8] |
Дополнительные доказательства взаимодействия СООН-групп Н - КМЦ с гидроксилами спиртов получены при изучении взаимодействия Н - КМЦ с этиловым спиртом и глицерином. [9]
Дополнительные доказательства справедливости уравнения ( 97) были получены при изучении изотопного обмена дейтерия. Очевидно, что если реакцию конденсации проводят в тяжелой воде D2O, в результате реакции, обратной ( 96а), дейтерий будет замещать протон ацетальдегида, приводя к образованию дейтерированного альдоля. Однако с уменьшением концентрации альдегида степень дейтерирова-ния должна возрастать. Исследуя кинетику рассматриваемой реакции в 10 М растворе альдегида, Бонхефер и Уолтере [143] подтвердили, что в этих условиях степень дейтерирова-ния альдоля действительно незначительна. Согласно результатам более недавней работы [144], где исследования проводились в растворе альдегида с концентрацией в интервале 0 05 - 1 4 М, эффективность дейтерирования увеличивается с понижением концентрации ацетальдегида, количественно согласуясь с приведенным выше механизмом. [10]
Дополнительные доказательства накопления микрокристаллических включений на границе раздела были получены в нашей лаборатории Г. Ф. Романовой и Р. И. Марченко с помощью масс-спек-трометрического метода анализа пиков ионно-ионной эмиссии. Первое связано с более трудным характером распыления упорядоченной фазы, а всплески примесных пиков - со свойством этого элемента накапливаться на границе раздела с кремнием. Микрофотографии примыкающей к границе раздела области окисла при стравливании окисла на клин подтверждают наличие ступенчатого рельефа оставшегося окисного слоя и характерных дефектов окисла вблизи границы раздела. [11]
Имеются также дополнительные доказательства в пользу теории, согласно которой ббльшая энергия заслоненных форм обусловлена отталкиванием между заместителями соседних атомов углерода. Так, у F3C - CF3 энергетический барьер равен 3 9 ккал / моль, а у С13С - СС13 - 10 ккал / молъ, что, несомненно, обусловлено большим объемом атомов хлора. В последнем соединении благодаря тому, что ковалентный радиус кремния намного больше радиуса углерода, атомы хлора так далеко отстоят друг OTjipyra, что между ними не существует заметного взаимодействия. [12]
Имеются также дополнительные доказательства в пользу теории, согласно которой ббльшая энергия заслоненных форм обусловлена отталкиванием между заместителями соседних атомов углерода. Так, у F3C - CF3 энергетический барьер равен 3 9 ккал / моль, а у С13С - СС13 - 10 ккал / моль, что, несомненно, обусловлено большим объемом атомов хлора. В последнем соединении благодаря тому, что ковалентный радиус кремния намного больше радиуса углерода, атомы хлора так далеко отстоят друг от друга, что между ними не существует заметного взаимодействия. [13]
Однако необходимы дополнительные доказательства этой точки зрения. [14]
Избегайте приводить дополнительные доказательства и данные для подтверждения выводов, которые делаются в Учебнике и в задачах; эти доказательства обязательно вызовут новые вопросы и тогда потребуется привести подробности из физики и химии, слишком сложные на данном этапе обучения. [15]
Страницы: 1 2 3 4