Смешанный контроль
Cтраница 3
В начале процесса катодная реакция протекает с диффузионным, а анодная - со смешанным диффузионно-электрохимическим контролем, затем анодная реакция нагаинает лимитироваться диффузией, а катодная протекает со смешанным контролем. [31]
Кинетический контроль суммарного процесса может определяться скоростями реакций ( I) или ( II), но может осуществляться и смешанный контроль. Один из способов определения времен жизни анион-радикала А базируется на переходе системы А - - Р or кинетического контроля одной из реакций ( I) или ( II) к смешанному контролю при изменении концентрации катализатора. [32]
Преимущественный контроль скоростью катодной реакции характерен для коррозии металлов в кислых средах, в нейтральных электролитах и атмосферных условиях, а также для коррозии амфотерных металлов в щелочных средах. Контроль скоростью протекания анодной реакции характерен для металлов, способных переходить в пассивное состояние. Смешанный контроль - контроль скоростями обеих реакций - наиболее распространен в практике и встречается в различных условиях, например при коррозии алюминия в нейтральных электролитах. [33]
После проделанного анализа можно сформулировать условия безопасности применения ингибиторов: анодные ингибиторы безопасны только в тех случаях, когда скорость коррозии контролируется всецело анодной реакцией. Плотность тока, возникающая на той части электрода, которая осталась по каким-либо причинам в активном состоянии, остается в таких условиях такой же, как и в исходном электролите. При смешанном контроле скорости коррозии анодные ингибиторы в концентрациях, не обеспечивающих полную пассивацию металла, вызывают увеличение интенсивности коррозии. Чем с большей поляризуемостью электрода протекает анодная реакция в исходном электролите, тем ниже интенсивность коррозии в присутствии ингибитора и тем менее опасным является такой ингибитор. Высокая катодная поляризуемость металла в исходном электролите, наоборот, способствует увеличению интенсивности коррозии в электролите, содержащем недостаточную для полной защиты концентрацию анодных ингибиторов. [34]
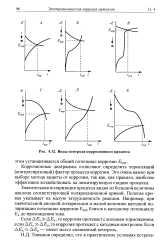 |
Виды контроля коррозионного процесса. [35] |
Кк, то коррозия протекает с анодным торможением, если А. ЕК А-Ба, то коррозия протекает с катодным контролем. ЕК ss АЕа - имеет место смешанный контроль. [36]
Значение Екор можно измерить с помощью электрода сравнения; измерить же / кор нельзя, так как в случае коррозионного элемента подключить в цепь амперметр практически невозможно. На рис. 1.11, б, в и г показано, как кинетика реакций позволяет установить скорость коррозии при катодном, анодном и смешанном контроле. [38]
 |
Изотермы термического окисления кремния в водяном паре при Ян О 1 атм. [39] |
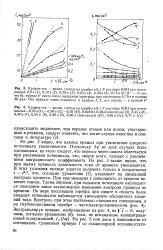
Величина энергии активации заметно зависит от состояния исходной поверхности кремния и наличия на ней хемосорбированных примесей того или иного типа. По эффективной энергии активации можно условно сделать вывод о наиболее медленно протекающей ( контролирующей) стадии процесса. При этом интервал 40 - 120 кДж / моль ( 10 - 30 ккал / моль) характеризует преимущественно диффузионный контроль, интервал 280 - 400 кДж / моль ( 70 - 100 ккал / моль) определяет преобладание поверхностной реакции, а промежуточные значения энергии активации отвечают смешанному контролю. [40]
Величина энергии активации заметно зависит от состояния исходной поверхности кремния и наличия на ней хемосорбированных примесей того или иного типа. По эффективной энергии активации можно условно сделать вывод о наиболее медленно протекающей ( контролирующей) стадии процесса. При этом интервал 40 - 120 кДж / моль ( 10 - 30 ккал / моль) характеризует преимущественно диффузионный конт - роль, интервал 280 - 400 кДж / моль ( 70 - 100 ккал / моль) определяет преобладание поверхностной реакции, а промежуточные значения энергии активации отвечают смешанному контролю. [41]
Из рис. 3 видно, что наклон прямых при увеличении анодного потенциала увеличивается. Поскольку Дер во всех случаях было одинаковым, из этого следует, что перенос через окисел облегчается при увеличении потенциала, что, скорее всего, связано с увеличением миграционного коэффициента. Из рис. 3 также видно, что при малых временах зависимость тока от времени уменьшается. В этих условиях прямые удается получить только в координатах i - t 5, что, согласно уравнению ( 7), указывает на смешанный контроль процесса. При еще меньших / зависимость от времени исчезает совсем. Таким образом, при заданном потенциале наблюдается описанное выше закономерное изменение контроля процесса во времени. По мере пассивации серебра при сдвиге в область более анодных потенциалов наблюдается уменьшение абсолютных значений тока. На рис. 5 они даны в зависимости от потенциала. [43]
Коэффициент диффузии в основном зависит от температуры, а также от природы реагентов и среды. Толщина диффузионного слоя уменьшается при перемешивании, соответственно перемешивание увеличивает скорость подвода реагентов. Если скорость диффузии ниже скорости реакции уд v, то процесс лимитируется диффузией. Если скорость диффузии достаточно высока уд v, то говорят о кинетическом контроле, т.е. процесс лимитируется собственно химической реакцией. Если va и V соизмеримы, то говорят о смешанном контроле. [44]
Из уравнений ( 7) - ( 9) видно, что при увеличении произведения ( Q. Vt) природа контроля должна закономерно изменяться от электрохимического к смешанному, а затем - к диффузионному контролю. Эта закономерность может быть использована для дополнительной проверки выводов, получаемых с помощью метода потенциостатической хроноамперометрии. Величину произведения для этого можно изменять, изменяя, например, Q ( практически потенциал электрода), и сравнивать данные, относящиеся к одинаковому моменту времени. Последний случай иллюстрируется схемой, взятой из [3] и приведенной на рис. 2, на которой видны все три области: при малых t - область электрохимического контроля, при средних - область смешанного контроля и, наконец, при достаточно больших t - область диффузионного контроля. [45]
Страницы: 1 2 3