Конфигурация - катион
Cтраница 1
Конфигурация фосфорсодержащего катиона - тетраэдрическая. [1]
Такая конфигурация катиона, по-видимому, создает в нем минимальные стерические препятствия, что проявляется в слабом искажении конформации циклов. [2]
Каталитическая активность окислов с конфигурацией катиона d5 и выше для последних двух реакций не изучалась. [3]
Типичные окислы - изоляторы второго малого периода и пятиокись фосфора ( все они имеют конфигурацию катионов Is22s22pe) можно использовать для иллюстрации ряда поверхностных свойств. Эффективные ионные заряды гораздо меньше формальных зарядов, приведенных в таблице ( за исключением MgO), но формальные величины ионных потенциалов позволяют перекинуть мостик к более старым ионным теориям и некоторым полезным корреляциям, например к корреляции с тенденцией к стеклованию. [4]
Участие всех групп пяти - или шестидентатного хеланта в координации невозможно также в случае комплексов, имеющих плоскостную структуру [57], обусловленную орбитальной конфигурацией катиона. Например, в нитрилтриацетате меди [40] Й5р2 - связь катиона с лигандом происходит за счет двух атомов кислорода карбоксильных групп и атома азота ( с. Четвертая координационная связь меди насыщается молекулой воды. Третья карбоксильная группа нитрилтриуксусной кислоты не принимает непосредственного участия в комплексообразовании из-за пространственных затруднений. [5]
Участие всех групп пяти - или шестидентатного хеланта в координации невозможно также в случае комплексов, имеющих плоскостную структуру [57], обусловленную орбитальной конфигурацией катиона. [6]
B окислах металлов с частично заполненными а-ободочкамк - fe 03, CoO Со50 СцО - - состояния у потолка валентной зоны принадлежат oi - состояниям катионов, 2р - зоны 0 расположены ниже в ряде случаев энергетически перекрываясь с а-зонами и проводимость осуществляется переносом электрона по состояниям а-характера Д, 2 8 /, Вследствие описанных особенностей энергетического строения в окислах с конфигурациями катионов о - или о. Си-зоне в форме катионов, имеющих степень окисления на единицу выше степени окисления катиона Е данном окисле, электроны в а-зоне проводимости в форме. Анион-радикалы 0 - обладают высокой реакционной способностью в реакциях окисления. [7]
Этот максимум приписывается атому кислорода молекулы воды. Конфигурация катиона [ AsPhJ 1 тетраэдрическая, связи имеют обычную длину. [8]
Итак, отношение равновесных концентраций зависит от разности свободных энергий образования изомеров. Как и в случае твердых растворов, изомер практически исчезает из равновесной смеси, если на его образование тратится работы на 7 - 8 ккал / моль больше, чем на образование более устойчивого изомера. При малых различиях в энергии ( как, например, у двух конфигураций катиона [ Си ( Н2О) 6 ] 2 - удлиненного и укороченного октаэдра ДО0 в водном растворе при комнатных температурах составляет 1 ккал / моль) концентрации обеих изомерных форм сопоставимы. [9]
Если предположить, что лимитирующей стадией реакции является адсорбция или иная стадия, сопровождающаяся увеличением координационного числа, то минимальный экзотермический эффект будет наблюдаться у систем du, d5, dw, которые имеют и минимальную каталитическую активность. Авторы [173] объясняют и некоторые исключения из этой простой закономерности. Например, переходы квадратная пирамида - октаэдр ( грань 100) на Соа03 ( конфигурация катиона de) и CuO ( d9), согласно данным табл. 2, сопровождаются эндотермическим эффектом. [10]
Хотя пока еще получено мало экспериментальных данных, подтверждающих существование простого соотношения между каталитической активностью окислов переходных металлов и числом с. Она представляется особенно важной, поскольку открывает также возможность более глубокой оценки полупроводниковых свойств. Много лет назад здесь была обнаружена некоторая аномалия, ибо если волновые Зй. NiO, так как незаполненные Зй8 - конфигурации катионов должны дать незаполненную зону. [11]
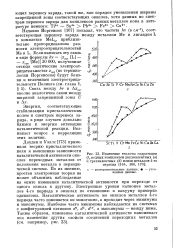 |
Изменение теплоты гидратации Qf водных комплексов двухвалентных ( а и трехвалентных ( б ионов металлов 4-го периода. [12] |
Дауден и Уэллс [173] применили теорию кристаллического поля к выяснению зависимости каталитической активности окислов переходных металлов от положения металла в периодической системе. По их мнению, простая электронная теория не может объяснить наблюдаемые на опыте изменения каталитической активности при переходе от одного окисла к другому. Электронные уровни катионов металлов 4-го периода в окислах по отношению к вакууму примерно одинаковы. Каталитическая активность же окислов металлов 4-го периода часто изменяется не монотонно, а проходит через минимумы и максимумы. Наиболее часто минимумы наблюдаются на системах с конфигурацией катионов d, d5, d10, а максимумы - между ними. [13]
Страницы: 1