Конфигурация - октаэдр
Cтраница 1
Конфигурации октаэдра, куба и тетраэдра относятся к кубическим группам симметрии. [1]
Комплексы 2Д - МХ4 имеют конфигурацию октаэдра ( рис. III.8), иногда сильно искаженного, причем возможно цис - и транс-расположение молекул Д в октаэдре. [2]
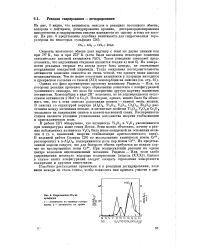 |
Гидрогенолиз CS, на сульфидах. [3] |
Однако это факт противоречит простому механизму Ридиела - Или, па которому реакция протекает через образование комплекса с конфигурацией удлиненного октаэдра, что дало бы совершенно другую картину изменения активности. Последнее, однако, можно было бы объяснить тем, что в этих окислах расстояния катион - катион очень велики. В окислах со структурой корунда ( А1203, Ti203, V303, Cr20s, Fea03) расстояния между катионами меньше, и магнитные свойства Ti203, У203и Cr20s указывают на спаривание спинов в катион-катионной связи. Неспаренность спинов является условием установления постоянства энергии стабилизации в кристаллическом поле. [4]
В соответствии с результатами структурных исследований ( см. рис. Ill А) для пятикоординационных комплексов Д - Т1С14 принята конфигурация тетрагональной пирамиды, для пятикоординационных комплексов Д-5 пХ4 - конфигурация тригональной бипирами-ды, для шестикоординационных комплексов тетрагалогенидов титана и олова - конфигурация октаэдра. [5]
Как отмечает SB I 41, квадратная конфигурация [ СиС14 ] - - иона отвечает представлениям теории направленных валентностей ( см. § § 94, 95), но, с другой стороны, две молекулы воды втянуты в координационную сферу узлов СпС14, так что формула соединения скорее имеет вид: К2 [ GuCl4 ( H20) 2 ], причем вокруг атома меди координационная сфера имеет конфигурацию октаэдра. Узлы а образуют тетрагональную центрированную ячейку, узлы ( 3 образуют призматическую координационную сферу вокруг узлов а, довернутую на 45 по отношению к оси ячейки. [6]
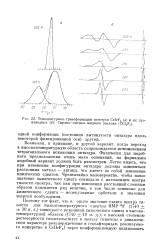 |
Температурные трансформации спектров CsIrFB ( а и их производных ( б. Справа-сигнал жидкого эталона ( CC12F2. [7] |
Возможен, в принципе, и другой вариант, когда переход в высокотемпературную область сопровождается исчезновением тетрагонального искажения октаэдра. Физически для подобного предположения очень мало оснований, но формально подобный вариант должен быть рассмотрен. Легко видеть, что при изменении конфигурации октаэдра должны изменяться расстояния металл - лиганд, что влечет за собой изменение химических сдвигов. Чрезвычайно маловероятно, чтобы новое значение химического сдвига совпадало с положением центра тяжести спектра, так как при изменении расстояний сложным образом изменяется ряд величин, в том числе основные для химического сдвига - молекулярные орбитали и значения энергий возбуждения. [8]
Прежде всего рассмотрим возможные конфигурации комплексов ионов ( П) переходного периода. На основании теории поля лигандов [6, 8] эти ионы могут образовывать всевозможные конфигурации комплексов с координационными числами от 2 до 7: линейную, плоскую, треугольную, тетра-эдрическую, тригональную бипирамидальную, октаэдричес-кую и пентагональную бипирамидальную. Если считать, что медь ( П) образует квадратные комплексы ( в соответствии с эффектом Яна - Теллера [6] для d9), то становится понятным равенство констант устойчивости ее комплексов с глицином и аминоизопропилфос-фоновой кислотой. Для всех остальных элементов наиболее вероятна конфигурация октаэдра. Тогда, в связи с тем, что молекула аминоизопропилфосфоновой кислоты занимает только два координационных места у ионов металлов, а в комплекс входят всего две такие молекулы, два остающиеся координационных места должны быть заняты молекулами воды гидратной оболочки иона. В силу стереохимии фосфоновой группы эти молекулы воды могут образовать водородные связи с ней, что и приводит к дополнительной стабилизации комплексов и увеличению их констант устойчивости. [9]
В то время как у мышьяка и фосфора координационное число разно 4, у сурьмы оно равно 6 и ее высшая кислородная кислота H7SbOe имеет иную форму, а поэтому и совершенно иные свойства, чем мышьяковая и фосфорная кислоты. Ее натриевая соль NaHeSbOe, ошибочно принимавшаяся ранее за пироантимонат, в аналитической химии используется как реактив на калий. Ее анион, как установлено структурным анализом, имеет конфигурацию октаэдра. Висмут стехио-метрически достаточно определенных соединений с валентностью 5 вообще не образует. [10]
В то время как у мышьяка и фосфора координационное число равно 4, у сурьмы оно равно 6 и ее высшая кислородная кислота H7SbO (; имеет иную форму, а поэтому и совершенно иные свойства, чем мышьяковая и фосфорная кислоты. H ( SbOi, ошибочно - принимавшаяся ранее за пироаитимонат, в аналитической химии используется как реактив на натрий. Ее анион, как установлено структурным анализом, имеет конфигурацию октаэдра. Висмут стехиометрически достаточно определенных соединений с валентностью 5 вообще не образует. [11]
Страницы: 1