Валентная электронная конфигурация
Cтраница 1
 |
Диаграмма состояния системы марганец - фосфор. [1] |
Валентная электронная конфигурация всех элементов VA-группы - ns2np3, т.е. на внешнем энергетическом ( валентном) уровне они содержат два спаренных ns - электрона и три неспаренных электрона на трехкратно вырожденном np - уровне. Однако между элементами этой группы существуют и различия в электронном строении. В силу наличия внутренних d - и / оболочек, экранирующих внешние электроны, в ряду As - Sb - Bi проявляется вторичная периодичность. В результате этого для среднего элемента ряда - сурьмы - степень окисления 5 оказывается более стабильной, чем для мышьяка и висмута. [2]
 |
Диаграмма состояния системы марганец - фосфор. [3] |
Валентная электронная конфигурация всех элементов VA-группы - ns2np3, т.е. на внешнем энергетическом ( валентном) уровне они содержат два спаренных ns - электрона и три неспаренных электрона на трехкратно вырожденном np - уровне. Однако между элементами этой группы существуют и различия в электронном строении. У мышьяка, сурьмы и висмута к вакантному пс ( - уровню добавляется еще в отличие от фосфора полностью завершенный внутренний ( п - 1) rf - уравень, а у висмута, следующего за лантаноидами, кроме того, и 4 / 4-уровень. В силу наличия внутренних d - и / оболочек, экранирующих внешние электроны, в ряду As - Sb - Bi проявляется вторичная периодичность. В результате этого для среднего элемента ряда - сурьмы - степень окисления 5 оказывается более стабильной, чем для мышьяка и висмута. [4]
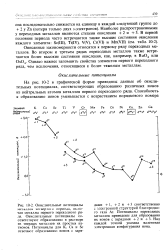
Над каждой точкой указана валентная электронная конфигурация иона. [6]
Таким образом, каждый период открывается щелочным металлом с валентной электронной конфигурацией: nsl. Завершается n - й период элементами, у которых наружные оболочки полностью заселены. [7]
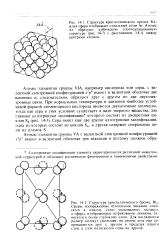
Атомы элементов группы VIA, например кислорода или серы, с валентной электронной конфигурацией s2p4 имеют в валентной оболочке две вакансии и, следовательно, образуют друг с другом по две двухэлек-тронные связи. [9]
При любых химических превращениях разрушаются валентные электронные оболочки исходных компонентов и синтезируются новые валентные электронные конфигурации продуктов реакции. [10]
ЭИВО определяют как энергию ионизации свободного атома или иона, усредненную по всем термам данной валентной электронной конфигурации. [11]
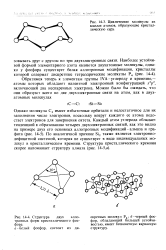 |
Циклические молекулы из восьми атомов, образующие кристаллическую серу.| Структура двух аллотропных форм кристаллического фосфора, а-белый фосфор, состоит из ди. [12] |
Обратимся теперь к элементам группы IVА - углероду и кремнию - атомы которых обладают валентной электронной конфигурацией s2p2, включающей два неспаренных электрона. [13]
Запишите орбитальные электронные конфигурации основного состояния Cl, С1 и Cl -, а также их валентные электронные конфигурации. [14]
К IVA-группе элементов, помимо типических, относятся элементы подгруппы германия: Ge, Sn и Pb. Их валентная электронная конфигурация ( ns np2 в невозбужденном состоянии) обусловливает возможность проявления свойств и катионо - и анионообразователей. Кроме того, эти элементы непосредственно примыкают к границе Цинтля справа и число валентных электронов достаточно для образования структур с ко-валентной связью у соответствующих простых веществ с координационными числами согласно правилу Юм-Розери 8 - N. Однако преимущественно ковалентная связь в кристаллах соединений в действительности реализуется далеко не всегда. [15]
Страницы: 1 2 3