Несвязывающая конфигурация
Cтраница 1
Несвязывающая конфигурация ( %) 6 отвечает шести электронам иона Со3 ( d6), не принимающим участия в образовании связи. [1]
По теории КП несвязывающая конфигурация ( nd) отвечает заполнению de - ор-биталей иона Со ( de), находящегося в сильном поле октаэдрической римметрии. [2]
Эти результаты, противоречащие изложенному выше, можно объяснить проявлением несвязывающих конфигураций и соответствующих энергий стабилизации поля лигандов. Вода имеет относительно слабое поле лигандов, и можно ожидать, что она будет образовывать спин-свободные комплексы, так что комплекс Со ( II) будет обладать fifedy - конфигурацией. С другой стороны, когда поле лигандов сильнее, как в случае цианид-ионов, следует ожидать образования спин-спаренных комплексов с dedY - конфигурацией. В этих условиях существует сильная тенденция к потере единственного электрона dy - орбитали с образованием комплекса Со ( III) в очень устойчивой dK - конфигурации. [3]
Структура соединений, в которых переходные элементы имеют координационное число 5, зависит от несвязывающей конфигурации металла. Если металл имеет малое или большое число электронов на несвязывающих ( п - 1) с. [4]
Несмотря на то что приведенные выше рассуждения безусловно очень важны, большую роль при определении относительных устойчивостей различных степеней окисления играет также несвязывающая конфигурация металла. Это наблюдается в химии кобальта. [5]
Приведенные выше соображения относятся только к правильным структурам. Под влиянием эффекта Яна - Теллера несимметричные несвязывающие конфигурации, например ds для Ni ( II), могут приводить в структуре неправильного тетраэдра, для которой энергетические уровни будут такими, как показано на рис. 7.8. Было отмечено, что соединения NiX2 ( PPh3) 2 ( где Х С1, Вг, I или МО3) имеют структуру искаженного тетраэдра ( Венанци, 1958), тогда как искажение в комплексе [ NiClj2 -, по-видимому, настолько мало, что им практически можно пренебречь. [6]
Медь, серебро и золото проявляют положительную степень окисления I, так как при этом осуществляется очень устойчивая несвязывающая - конфигурация. Из правил Хунда следует, что наиболее устойчивыми несвязывающими конфигурациями являются те, в которых каждая из вырожденных орбгогалей будет: а) полностью свободной, б) занятой одним электроном, в) занятой двумя электронами с противоположными спинами. [7]
Известно, что непереходные элементы образуют производные с алкилами, очень похожие на другие соединения этих элементов, например на галогениды. Так, сильно основные щелочные металлы образуют ионные алкилы ( ср. Большинство переходных элементов не образуют таких галогенидов: так, хлорид Fe ( III) более устойчив, чем гексакво-комплекс [ Ре ( Н2О) е ] С1з, в котором металл имеет координационное число, равное 6, и даже в безводном состоянии структура его полимерна, а металл сохраняет это значение координационного числа. Устойчивость правильного октаэдрического расположения вокруг Fe ( III) объясняется наличием у металла несвязывающей конфигурации, которая симметрична относительно октаэдрического поля лигандов. [8]
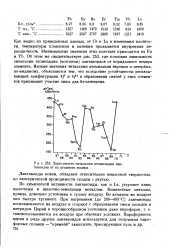 |
Зависимость энтальпии атомизации лантаноидов от их атомного номера. [9] |
Как видно из приведенных данных, от Се к Lu в изменении плотности, температуры плавления и кипения проявляется внутренняя периодичность. Минимальные значения этих констант приходятся на Ей и Yb. Об этом же свидетельствует рис. 253, где показана зависимость энтальпии атомизации ( возгонки) лантаноидов от порядкового номера элемента. Низкие значения энтальпии атомизации европия и иттербия, по-видимому, объясняются тем, что вследствие устойчивости несвязывающей конфигурации 4 / и 4 / 4 в образовании связей у этих элементов принимают участие лишь два б - электрона. [10]
Как видно из приведенных данных, от Се к Lu в изменении плотности, температуры плавления и кипения проявляется внутренняя периодичность. Минимальные значения этих констант приходятся на Ей и Yb. Об этом же свидетельствует рис. 248, на котором показана зависимость энтальпии атомизации ( возгонки) лантаноидов от порядкового номера элемента. Низкие значения энтальпии атомизации европия и иттербия, по-видимому, объясняются тем, что вследствие устойчивости несвязывающей конфигурации 4 / 7 и 4f14 в образовании связей у этих элементов принимают участие лишь два бх-элек-трона. [11]
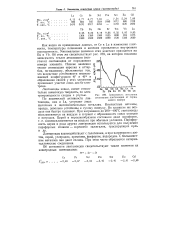 |
Зависимость энтальпии атомизации лантаноидов от порядкового номера. [12] |
Как видно из приведенных данных, от Се к Lu в изменении плотности, температуры плавления и кипения проявляется внутренняя периодичность. Минимальные значения этих констант приходятся на Ей и Yb. Об этом же свидетельствует рис. 239, на котором показана зависимость теплот атомизации ( возгонки) лантаноидов от порядкового номера элемента. Низкие значения теплот атомизации европия и иттербия, по-видимому, объясняются тем, что вследствие устойчивости несвязывающей конфигурации 4 / 7 и 4 / 14 в образовании связей у этих элементов принимают участие лишь два Gs-элек-трона. [13]
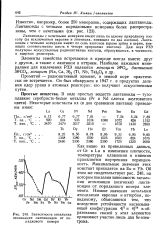 |
Зависимость энтальпии атомизации лантаноидов от порядкового номера. [14] |
Как видно из приведенных данных, от Се к Lu в изменении плотности, температуры плавления и кипения проявляется внутренняя периодичность. Минимальные значения этих констант приходятся на Ей и Yb. Об этом же свидетельствует рис. 248, на котором показана зависимость энтальпии атомизации ( возгонки) лантаноидов от порядкового номера элемента. Низкие значения энтальпии атомизации европия и иттербия, по-видимому, объясняются тем, что вследствие устойчивости несвязывающей конфигурации 4 / 7 и 4 / 14 в образовании связей у этих элементов принимают участие лишь два Gs-элек-трона. [15]
Страницы: 1