Конформация - белковая молекула
Cтраница 1
Конформация белковых молекул оказывает решающее влияние на величину связывания углеводорода. [1]
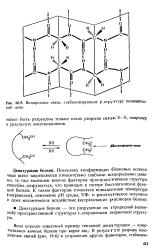 |
Водородные связи, стабилизирующие р-структуру попипептид-ной цепи. [2] |
Поскольку конформации белковых молекул чаще всего закрепляются относительно слабыми водородными связями, то под влиянием многих факторов пространственная структура способна разрушаться, что приводит к потере биологических функций белков. [3]
Как известно, конформацию белковой молекулы можно нарушить посредством какого-либо внешнего воздействия. Такое нарушение ведет к увеличению объема молекулы, что проявляется в снижении объема выхода. Вполне возможно, что часть молекул денатурировалась и занимает поэтому больший объем. Так, молекулярный вес ри-бонуклеазы, установленный на сефадексе G-100, увеличивается после денатурации щелочью в 1 9 раза, после окисления надмуравьинои кислотой - в 3 0 раза, после обработки 4 М мочевиной - в 2 5 раза, а после обработки 8 М мочевиной - в 4 3 раза. Как можно убедиться с помощью гель-фильтрации на сефадексе G-200 [160], химическая модификация сывороточного альбумина ( ацилирование различными реагентами) приводит к весьма значительному увеличению объема. [4]
На последнем этапе формируется на-тивная конформация белковой молекулы, связанная с замыканием дисульфидных связей и окончательной стабилизацией белко - 3.10. Нативная структура вой конформации. [5]
Очень чувствительным методом исследования конформации белковых молекул и синтетических полипептидов является изучение оптической активности и в особенности дисперсии врэ-щения. [6]
В частности, устойчивость на-тивной конформации белковых молекул обусловлена определенной последовательностью расположения гидрофобных аминокислотных остатков в полипептидной цепочке. [7]
При таком разрыве связи изменяется конформация белковой молекулы. Происходит это таким образом, что группы, участвующие в механизме каталитического акта, принимают нужную ориентацию в пространстве. Связывающий и каталитический участки составляют активный центр вместе и, следовательно, они должны находиться поблизости друг от друга или перекрываться. Поскольку связывающий участок, как мы видели, уже имеется в проферменте, то ясно, что конформационные изменения, необходимые для создания каталитического участка и происходящие при активации, должны быть сосредоточены на очень небольшом отрезке молекулы. [8]
Поперечные дисульфидные мостики помогают уберечь дативную конформацию белковой молекулы от денатурации. [9]
В заключение необходимо отметить, что в обоих рассмотренных случаях характерная конформация белковой молекулы, обусловленная специфическим распределением внутренних связей, приводит к наличию необычайно реакционноспособных участков. [10]
Механизм образования этой высокоупорядоченной структуры из первоначально вязкой нефибриллярной секреции гусеницы и конформация белковых молекул до начала прядения щелка пока не установлены. [11]
Гидролазы относятся к ферментам, у которых активная группа образована в результате особой конформации белковой молекулы. При изгибах полипептидной цепи белка некоторые аминокислотные остатки сближаются и их сочетание образует активный центр биологического катализатора. Высказывалось мнение, что строгая специфичность фермента ( его узкая специальность - настроенность только на определенную реакцию) зависит от окружения активной группы. [12]
Ионообменный процесс может привести к частичной или полной инактивации фермента вследствие значительного изменения рН или конформации белковой молекулы. [13]
Полученный в работе экспериментальный материал показывает, что измерение эффекта солюбилизации может служить методом для определения конформации белковых молекул в растворе, а именно третичной структуры. [14]
В результате кооперативных эффектов взаимодействий этих групп ( внутримолекулярных с молекулами внешней среды) и их частичной ионизации трехмерная конформация белковой молекулы и распределение зарядов на ее поверхности подвержены динамическим флуктуациям. [15]
Страницы: 1 2