Концентрация - свободный анион
Cтраница 1
Концентрация свободных анионов Y4 - в кислых растворах комплексона ЭДТА практически ничтожно мала. [1]
Концентрация свободных анионов Y - в кислых растворах комплексона ЭДТА практически ничтожно мала. [2]
Концентрацию свободного аниона удается установить прямыми измерениями в тех случаях, когда анион образует с катионами металла электрода труднорастворимую соль, что позволяет создать электрод второго рода. Каломельный и хлорсеребряный электроды - наиболее распространенные вспомогательные полуэлементы - могут быть применены для определения концентрации ионов хлора [ 63, гл. [3]
В этом случае концентрация свободного аниона R очень сильно зависит от рН раствора. [4]
Решение задачи нахождения концентрации свободного аниона упростится, как только будет разработан широкий набор мембранных электродов с анионными функциями. В этом направлении интенсивно ведутся исследования и достигнуты определенные успехи [ 3, дополн. Концентрация свободного аниона, в том числе иона гидроксила, может быть вычислена с помощью экспериментальной величины рН, если значение константы диссоциации кислоты в условиях опыта известно. [5]
При увеличении рН растет и концентрация свободных анионов. Такие явления описаны для многих случаев, например для салицилата меди, ализаринат-ных комллексов, комплекса алюминия с эриохромцианином. [6]
При увеличении рН раствора растет концентрация свободного аниона реактива; это может, в свою очередь, привести к образованию комплексов с большим координационным числом и другой окраской. [7]
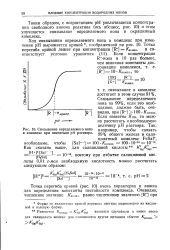 |
Связывание определяемого иона в комплекс при изменении рН раствора. [8] |
Таким образом, с возрастанием рН увеличивается концентрация свободного аниона реактива ( ось абсцисс, рис. 10) и этим улучшается связывание определяемого иона в окрашенный комплекс. [9]
 |
Связывание определяемого иона в комплекс при изменении рН раствора. [10] |
Таким образом, с повышением рН увеличивается концентрация свободного аниона реактива ( рис. 31) и этим улучшается связывание определяемого иона в поглощающий свет комплекс. [11]
В подобных системах изменение рН приводит к резкому изменению концентрации свободных анионов, способных к комплексообразованию с металлом. Дальнейшие осложнения связаны с тем, что некоторые лиганды способны протонироваться и в координированном состоянии. Протекание таких процессов сильно затрудняет трактовку данных по ионному обмену, так что количественное исследование комплексообразования оказывается возможным лишь в некоторых отдельных случаях. [12]
Если комплексообразующиу реагентом является слабая кислота, например лимонная, то концентрация свободных анионов зависит не только от общей концентрации промывного раствора, но и от рН раствора. [13]
Применение в качестве растворителя ацетона ( 8 20 7) сдвигает равновесие ( 259) вправо, увеличивая концентрацию свободных анионов. [14]
Количество ионов Н в растворе ( практически в небуферных растворах равное полной концентрации кислоты [ А ] о) в экспериментах Гхоша было гораздо выше, чем полное количество ионов уранила. Следовательно, концентрация свободных анионов кислоты определяется ( в основном или исклю-чительно) концентрацией i [ A ] n и констянтпй диггпттияпин Г), я концентрация комплексов уранила, в свою очередь, определяется концентрацией свободных анионов кислоты. [15]
Страницы: 1 2