Концентрация - иодид
Cтраница 1
Концентрация иодида не должна быть высокой и должна составлять 1 - 3 мг / мл. [1]
При концентрации иодидов ниже 0 01 М индий не соосаждается. [2]
При концентрации иодида калия ниже 3 % окраска изменяется; при увеличении концентрации иодида окрашивание становится постоянным. Под действием окислителя, который может находиться в анализируемом растворе, или кислорода воздуха комплекс разрушается и из раствора выделяется свободный иод; этого можно избежать, если добавить в раствор восстановитель: аскорбиновую кислоту, сульфит, либо гипосульфит, либо смесь обоих реагентов. [3]
Диапазон концентраций иодидов, которые можно определить по варианту В, зависит от выбранных условий реакции. Если проба содержит иодиды в малых концентрациях, ее можно сконцентрировать упариванием при рН больше 7; при слишком высоких концентрациях иодидов в пробе ее разбавляют дистиллированной водой, свободной от иодидов. [4]
Для определения концентрации иодида в природных водах может быть применена методика, основанная на каталитическом действии иодида в другой окислительно-восстановительной реакции: окисление роданида нитратом натрия. Скорость реакции измеряется по изменению в единицу времени оптической плотности растворов, окрашенных рода-нидным комплексом железа. [5]
Исследование изменения концентрации иодида LXIX от концентрации трет. Порядок реакции при соотношениях до 2 молей трет. LXIX является первым по иодиду. [6]
Иначе говоря, концентрация иодидов равна 1 4 10 6 концентрации хлоридов. Это весьма важный фактор, позволяющий количественно титровать иодид-ион в присутствии хлорид-иона, используя подходящий адсорбционный индикатор или серебряный электрод. [7]
По мере роста концентрации иодида водорода реакция замедляется и, как правило, совсем прекращается еще до израсходования всего метилиодида. Такое влияние кислотности на изменение конфигурации комплексов родия мы обсудим в разд. [8]
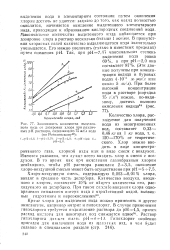 |
Зависимость количества выделенного иода от дозировки хлора при различных рН раствора, содержащего 75мг / л иода ( по Рогозинскому49. [9] |
Эти данные получены при концентрации иодида в буровых водах4 - 1СГ5 м-же 1л или около 5 мг. [10]
Эти исследования показали, что концентрация иодида калия в растворе должна быть не менее 4 % - ной, а значение рН ниже 4, потому что при более высоких рН образование основных солей меди ( II) приводит к медленному и неполному окислению иодид-иона. [11]
В работе [239] исследовано влияние концентрации иодида калия при постоянной концентрации серной кислоты ( 1 5 и 2 5 М) и влияние концентрации серной кислоты при постоянной концентрации иодида калия ( 6 5 - 10 - 3; 10 - 3 и 10 1 М) на экстракцию висмута изо амилацетатом. [12]
Существенное значение для протекания реакции (13.15) имеет концентрация иодида, которая в 4 - 5 раз должна превышать требуемую по стехиометрии, и кислотность раствора, хотя концентрация иона водорода и не входит в явном виде в уравнение реакции. Необходимо создание слабокислой среды, так как в нейтральных растворах ионы Си2 гидролизуются, а продукты гидролиза реагирут с иодидом очень медленно, что удлиняет процесс титрования и затрудняет фиксирование точки эквивалентности. В сильнокислых растворах ( [ Н ] 0 3 моль / л) происходит индуцированное медью окисление иодида кислородом воздуха, что приводит к получению завышенных результатов. [13]
Особенно вероятна потеря иода вследствие испарения, если концентрация иодида слишком мала и в системе содержится твердый иод. Для уменьшения концентрации свободного иода до значения ниже предела насыщения раствор должен содержать достаточное количество иодида. Испарение свободного иода увеличивается при выделении газов ( например, диоксида углерода при деаэрации) и при нагревании. Поэтому определения с использованием растворов иода следует проводить, применяя холодные растворы. [14]
Установлено, что тангенс угла наклона кривой зависимости концентрации иодидов от продолжительности реакции пропорционален концентрации молибдена. [15]
Страницы: 1 2 3 4