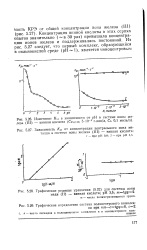
Концентрация - ион - железо
Cтраница 3
При применении аммиачного буферного раствора, 10-кратном избытке аскорбиновой кислоты и концентрации ионов железа - 15 мкг / мл комплекс образуется в течение 1 - 2 мин. Комплекс проявляет лишь незначительные отклонения от закона Бера при концентрации ионов железа выше 30 мкг / мл. [31]
Как следует из данных, представленных в табл. 2, при концентрации иона железа в растворе от 6 до 21 г / л обменная емкость слабоосновных мембран МАК значительно выше емкости мембран МАК-В и МКК. С уменьшением концентрации иона железа в растворе емкость мембран МАК убывает, мембран МАК-В - не изменяется до концентрации иона железа в растворе 1 г / л, после чего также убывает, а у мембран МКК постепенно возрастает. [32]
Возможность превращения Fe2 в Fe3 без образования ОН в случае повышения концентрации ионов железа открывает перспективы замены загрязняющих среду окислителей экологически чистым пероксидом водорода. Так, при производстве витамина С с использованием гипохлорита в качестве окислителя на тонну аскорбиновой кислоты образуется более 10 тонн хлористого натрия, попадание которого в окружающую среду приводит к минерализации природных вод и засолению почвы. [33]
Следующие вещества, присутствуя в концентрации, в 250 раз превышающей концентрацию ионов железа, могут привести лишь к ошибке, которая не будет больше 2 %: ацетат -, арсенат -, бромид - цитрат -, хлорид -, нитрат -, сульфат - и тар-трат-ионы, синильная, муравьиная, фосфорная и кремневая кислоты, ионы алюминия. [34]
Следующие вещества, присутствуя в концентрации, в 250 раз превышающей концентрацию ионов железа, могут привести лишь к ошибке, которая не будет больше 2 %: ацетат -, арсенат -, бромид -, цитрат -, хлорид -, нитрат -, сульфат - и тартрат-ионы, синильная, муравьиная, фосфорная и кремневая кислоты, ионы алюминия. [35]
Расчет защитного потенциала по этой формуле может быть выполнен только после определения концентрации ионов железа в слое электролита, непосредственно прилегающем к поверхности катодно защищаемого металла. Однако методов определения концентрации потенциалопределяющих ионов еще нет, если не считать попыток Березиной и др. Дополнительные затруднения возникают при экспериментальной проверке рассчитанных теоретически защитных потенциалов из-за недостаточной точности определения скорости коррозии при значительном смещении потенциала в отрицательном направлении от стационарного. [36]
Концентрация винной кислоты в этих сериях опытов значительно ( - в 30 раз) превышала концентрацию ионов железа и поддерживалась постоянной. [38]
Однако она протекает медленно, так что в точке эквивалентности обеспечивается достаточно высокая для реакции с индикатором концентрация ионов железа. При стоянии, и быстрее - при нагревании оттитрованного раствора коричневая окраска сали-цилата железа снова бледнеет. Значение рН в точке эквивалентности должно сохраняться в узких пределах. Если, с другой стороны, значение рН слишком низко, то приведенная выше реакция ускоряется и, таким образом, прибавляемое железо лишь вытесняет алюминий из его комплексоната. [39]
Анализ уравнения (5.27) показывает, что парциальное давление сероводорода ( концентрация сероводорода в газе) прямо пропорционально квадрату концентрации ионов железа. Поэтому повышение рН раствора за счет добавления щелочи является более эффективным методом снижения парциального давления сероводорода, чем повышение концентрации ионов железа. [40]
Скорость растворения железа в растворе, не содержащем его ионов, возрастает с повышением интенсивности перемешивания, приводящего к уменьшению концентрации ионов железа вблизи электрода. Однако в условиях промышленной эксплуатации электролизеров снижение скорости циркуляции электролита обычно вызывает усиление коррозии стальных деталей, что объясняется наличием большого количества примесей железа в технических электролитах. Кроме того, усиление циркуляции электролита уменьшает возможность обеднения его щелочью в отдельных зонах электролитической ячейки, благодаря чему уменьшается коррозия анодно работающих деталей. [41]
Полагая aFe2 / aCd2 mFe2 / mcd2 нах дим, что при концентрации ионов кадмия приблизительно в 18 раз меньшей, чем концентрация ионов железа, железо не вытесняет кадмий из раствора. Если же отношение / nCd2 / mFe2 меньше 1 / 18, то кадмий вытесняет железо. Сравнение элементов, далеко отстоящих один от другого в таблице стандартных потенциалов, показывает, что обращение реакции вытеснения часто практически невозможно. [42]
Напротив, когда марганец в металле практически отсутствует, то частичная замена FeO на МпО может быть реализована в условиях относительного преобладания концентрации ионов железа. В этом случае значения Z / лежат по другую сторону максимума кривой, где рост коэффициента - у преобладает над падением концентрации Npe2 - Тогда добавки МпО в шлак уменьшают содержание фосфора в металле. [43]
Изменению скачка потенциала на границе металл-раствор и сдвигу равновесного потенциала электрода в отрицательную сторону способствуют также ионы сульфидов в растворе, которые понижают концентрацию ионов железа в приэлектродном слое. Все это вместе взятое приводит к уменьшению поляризации железного электрода и облегчению протекания катодного и анодного процессов растворения металла. [44]
Вуд и Ремейка [79] исследовали эти реакции, используя поглощение света в области 1 14 мкм, которое, как было показано, пропорционально концентрации ионов железа с валентностью, не равной трем. Ионы Са2 и Si4 - обычные примеси, попадающие в кристаллы из исходного реактива и из футеровки муфельной печи. Показано, что, как и должно быть, гранат, активированный Са2, имеет р-тип проводимости, тогда как гранат, активированный Si, - и-типа. [45]
Страницы: 1 2 3