Концентрация - ион - кадмий
Cтраница 1
Концентрация ионов кадмия в электролите сильно влияет на состав катодного осадка. Так, при г к 1 А / дм2 и CCd: CNi 1: 6, содержание никеля в сплаве составляет - 20 %, а при cd: CNj 2: 6 на катоде выделяется только кадмий. С увеличением концентрации гликоля в электролите содержание никеля в сплаве и т к падают. Гликоль являясь донором водорода, обеспечивает у катода постоянное значение рН и доля тока, идущего на разряд ионов никеля, уменьшается. [1]
Для измерения концентрации ионов кадмия, меди, мышьяка, теллура, свинца, сурьмы, хрома, цинка и других элементов, а также органических веществ в водных растворах. [2]
Здесь [ Cd2 ] - концентрация ионов кадмия в массе раствора откуда ионы кадмия диффундируют, и [ Cd2 ] 0 - концентрация ионов кадмия в слое, окружающем электрод. [3]
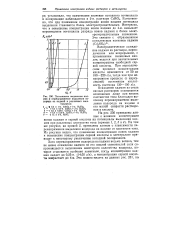 |
Потенциалы выделения кадмия и перенапряжение выделения водорода а - кадмий в - различны электролитах. [4] |
Естественно, что при понижении концентрации ионов кадмия потенциал выделения становится более электроотрицательным. [5]
Вычислить потенциал кадмия, погруженного в раствор с концентрацией иона кадмия 0 005 г-ион / л при 25 С. [6]
Равновесную концентрацию ионов кадмия в растворе рассчитывали, вычитая изначальной концентрации ионов кадмия то количество их, которое связано введенной щелочью. [7]
 |
Подпрограммы на фоне 0 1 М раствора КС1. [8] |
Высота волны кадмия ( h) составляет 66 мм и соответствует концентрации ионов кадмия 1 10 s г-ион / л; А. [9]
Полагая aFe2 / aCd2 mFe2 / mcd2 нах дим, что при концентрации ионов кадмия приблизительно в 18 раз меньшей, чем концентрация ионов железа, железо не вытесняет кадмий из раствора. Если же отношение / nCd2 / mFe2 меньше 1 / 18, то кадмий вытесняет железо. Сравнение элементов, далеко отстоящих один от другого в таблице стандартных потенциалов, показывает, что обращение реакции вытеснения часто практически невозможно. [10]
Рассчитать ток, проходящий через полярографическую ячейку при потенциале - 0 55 В ( н.к.э.), если концентрация ионов кадмия в растворе равна 240 мг / л, а коэффициент диффузии Cd2 равен 7 15 - 10 - 6 см2 - с-1. Период капания для капилляра равен 3 16 с, масса 50 капель ртути равна 0 168 г, температура 298 2 К. [11]
Здесь [ Cd2 ] - концентрация ионов кадмия в массе раствора откуда ионы кадмия диффундируют, и [ Cd2 ] 0 - концентрация ионов кадмия в слое, окружающем электрод. [12]
Для осаждения какого-нибудь сульфида, например CdS, необходимо, чтобы произведение молярных концентраций Cd 1 1 и S в растворе стало численно ббльшим, чем константа произведения растворимости CdS. Концентрацию ионов кадмия ( Сси) легко вычислить. [13]
Одновременно проводят контрольный опыт с 5 мл чистого подсолнечного масла, выдержанного в тех же условиях, что и вытяжка. Концентрацию иона кадмия определяют по градуировочному графику. [14]
Поскольку восстановление ионов кадмия протекает быстро и обратимо, концентрация их в слое раствора, окружающем электрод, в любой момент определяется потенциалом кадмиевого электрода. При изменении потенциала мгновенно изменяется и концентрация ионов кадмия в приэлектродном слое в соответствии с уравнением Нернста, что приводит либо к выделению металлического кадмия на электроде, либо к растворению электрода. [15]
Страницы: 1 2